
【题目】(1)有下列五种物质:
A. O2和O3
B.![]() 和
和![]()
C.CH3COOCH2CH3和CH3COOCH3
D.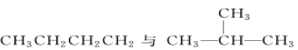
E. 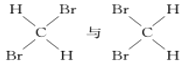
①________组两种物质互为同位素; ②________组两种物质互为同素异形体;
③________组两种物质互为同系物; ④________组两种物质互为同分异构体;
⑤________组两种物质为同一种物质;
(2)现有六种有机物:
A. CH3OH B.(CH3)3CCH2OH C.(CH3)3COH
D. (CH3)2CHOH E. C6H5CH2OH F. (CH3)2CHCl
①能被氧化铜氧化生成醛的有________。
②能被氧化铜氧化成酮的有________。
③能发生消去反应生成烯烃的有________。
(3)现有四种有机物:
A. (CH3)2CHCl B. CH3COOCH C. OHCCH2COOH D. CH3COOCH3
①能与新制Cu(OH)2反应的有________。
②能与NaOH水溶液反应的有________。
【答案】B A C D E ABE D CDF BC ABCD
【解析】
(1)同位素是指质子数相同,中子数不同的同种元素的不同核素;同素异形体是指同一种元素组成的不同种单质;同分异构体是指分子式相同,结构不同的化合物;同系物是指结构相似,分子组成上相差若干个CH2的有机物;据此分析解答;
(2)根据与羟基相连的碳含H原子的个数判断被催化氧化生成的产物,根据与卤素原子或羟基相连的碳的邻位碳上是否含H原子判断是否发生消去反应生成烯烃;
(3)结合官能团的性质分析解答。
(1)A.O2和O3为O元素组成的不同种单质,两者互为同素异形体;
B.![]() 和
和![]() 为Cl元素的两种核素,质子数相同,中子数不同,互为同位素;
为Cl元素的两种核素,质子数相同,中子数不同,互为同位素;
C.CH3COOCH2CH3和CH3COOCH3均属于酯类,分子组成上相差1个CH2,互为同系物;
D.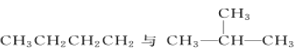 分子式均为C4H10,结构不同,互为同分异构体;
分子式均为C4H10,结构不同,互为同分异构体;
E.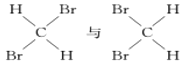 均是二溴甲烷,属于同一种物质;
均是二溴甲烷,属于同一种物质;
故答案为:B;A;C;D;E;
(2)A.CH3OH与羟基相连的碳上只有3个H原子,可被氧化铜催化氧化生成甲醛,不能发生消去反应;
B.(CH3)3CCH2OH与羟基相连的碳上有2个H原子,可被氧化铜催化氧化生成(CH3)3CCHO,与羟基相连的碳的邻位碳上没有H原子,不能发生消去反应生成烯烃;
C.(CH3)3COH与羟基相连的碳上没有H,不能生成醛,也不能生成酮,与羟基相连的碳的邻位碳上有3个H原子,可以发生消去反应生成CH2=C(CH3)2;
D.(CH3)2CHOH与羟基相连的碳上只有1个H原子,可被氧化铜催化氧化生成CH3COCH3,与羟基相连的碳的邻位碳上有3个H原子,可以发生消去反应生成CH2=CHCH3;
E.C6H5CH2OH与羟基相连的碳上有2个H原子,可被氧化铜催化氧化生成C6H5CHO,与羟基相连的碳的邻位碳上没有H原子,不能发生消去反应生成烯烃;
F.(CH3)2CHCl不被氧化铜催化氧化,与氯原子相连的碳的邻位碳上有3个H原子,可以发生消去反应生成CH2=CHCH3;
故答案为:ABE;D;CDF;
(3)①含有醛基或羧基的化合物能与新制Cu(OH)2反应,则符合条件的有CH3CH2OOCH和OHCCH2COOH,故答案为:BC;
②含有羧基或酯基或卤素原子的化合物能与氢氧化钠溶液反应,则能与NaOH水溶液反应的有(CH3)2CHCl、CH3CH2OOCH、OHCCH2COOH、CH3COOCH3,故答案为:ABCD。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铁触媒是重要的催化剂,CO易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5;除去CO的化学反应为:[Cu(NH3)2]OOCCH3+CO+NH3=[Cu(NH3)3(CO)]OOCCH3,
(1)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是_____,与CO互为等电子体的分子的电子式为______________。
(2)硝酸钾中NO3-的空间构型_____,与NO3-互为等电子体的一种非极性分子化学式为_____。
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型是________,配位体中提供孤对电子的原子是________。
(4)用[Cu(NH3)2]OOCCH3除去CO的反应中,肯定有______形成.
a.离子键 b.配位键 c.非极性键 d.σ键
(5)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示,

写出该反应的化学方程式____________________。 若两个最近的Fe原子间的距离为s cm,则该晶体的密度是__________g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
|
| ||||
相对分子质量 | 密度/(g/cm-3) | 沸点/℃ | 水中溶解性 | ||
异戊醇 | 88 | 0.8123 | 131 | 微溶 | |
乙酸 | 60 | 1.0492 | 118 | 溶 | |
乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 | |
实验步骤:在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min,反应液冷至室温后倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g。回答下列问题:
(1)仪器B的名称是__。
(2)在洗涤操作中,第一次水洗的主要目的是__;第二次水洗的主要目的是__。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后___(填标号)。
A.直接将乙酸异戊酯从分液漏斗的上口倒出
B.直接将乙酸异戊酯从分液漏斗的下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是__。
(5)在蒸馏操作中,仪器试剂的选择及安装都正确的是__(填标号)。
A.  B.
B.
C. D.
D.
(6)本实验的产率是__。
(7)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏__(填“高”或“低”),其原因是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.实验室将少量Na保存在乙醇中
B.可用激光笔鉴别FeCl3溶液和Fe(OH)3胶体
C.32 g O3中含有的氧原子数约是3×6.02×1023
D.常温下,可以用铝制容器来储运浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:
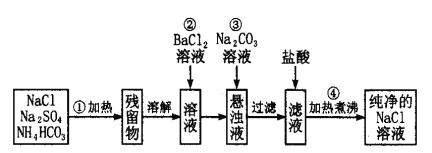
请回答下列问题:
(1)操作①可在什么仪器中进行?(填序号)__________。
A. 烧瓶 B. 坩埚 C. 容量瓶
(2)操作②发生的离子反应方程式为______________________________。
(3)操作②是否可改为加硝酸钡溶液?为什么?______________________。
(4)进行操作②后,如何判断SO42-已除尽,方法是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法回收WC和制备Co2O3的工艺流程简图如下:
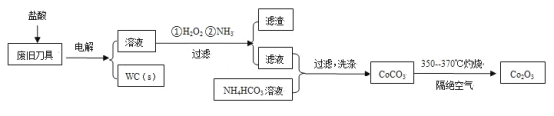
已知:在上述流程中,各种金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Co2+ |
开始沉淀的pH | 1.9 | 7.0 | 6.5 |
沉淀完全的pH | 3.2 | 9.0 | 9.4 |
回答下列问题:
(1)以废旧刀具作阳极,不锈钢作阴极,盐酸为电解质溶液。电解时阳极的电极反应有:Co-2e-=Co2+和______。
(2)通入氨气的目的是调节溶液的pH,除去铁元素。由表中的数据可知,理论上可选择的pH的范围是_______。
(3)生成CoCO3的离子方程式是________。
(4)实验测得NH4HCO3溶液显碱性。制备CoCO3时,不能将滤液加入NH4HCO3溶液中,原因是_______。
(5)已知:Ksp(CoCO3)=1.4×10-13,Ksp(CoC2O4)=6.3×10-8。若仅从沉淀转化角度考虑,在0.01mol/L Na2C2O4溶液中加入CoCO3固体能否转化为CoC2O4沉淀?通过计算说明:_________。
(6)洗涤CoCO3不充分对最终产品纯度并无影响,但在焙烧时会造成环境污染,主要原因是____。
(7)CoCO3生成Co2O3的化学方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2-二溴乙烷的反应原理如下所示:
第一步:CH3CH2OH![]() CH2=CH2+H2O;
CH2=CH2+H2O;
第二步:乙烯与溴水反应得到1,2-二溴乙烷。
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃下脱水生成乙醚(CH3CH2OCH2CH3)。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示(部分装置未画出):

有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/(g/cm3) | 0.79 | 2.2 | 0.71 |
沸点/(℃) | 78.5 | 132 | 34.6 |
熔点/(℃) | -130 | 9 | -116 |
请回答下列问题:
(1)写出乙烯与溴水反应的化学方程式:______。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_____(填字母代号)。
a.引发反应 b.加快反应速率
c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是______。
(4)在装置C中应加入____ (填字母代号),其目的是吸收反应中可能生成的SO2、CO2气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___ (填“上”或“下”)层。
(6)若产物中有少量副产物乙醚,可用____的方法除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 摩尔盐
摩尔盐![]() 在
在![]() 时分解生成
时分解生成![]() 、
、![]() 和
和![]() 等。某小组称取mg样品进行如下实验
等。某小组称取mg样品进行如下实验![]() 尾气处理装置省略
尾气处理装置省略![]() ,验证它的分解产物。
,验证它的分解产物。
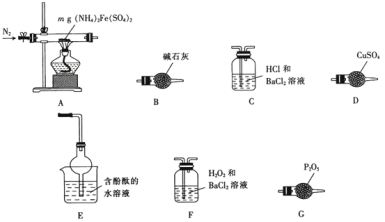
下列说法正确的是![]()
![]()
A.C中盐酸的作用是增强酸性,可以用硝酸替代盐酸
B.装置按![]() 连接可以检验
连接可以检验![]() 、
、![]() 、
、![]()
C.若实验中C、F都产生白色沉淀,则发生的反应不同,沉淀成分相同
D.实验完毕后,称量A中硬质玻璃管总质量,可以确定![]() 中x、y的值
中x、y的值
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com