
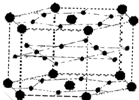
 A��B��C��D��E��F����Ԫ�أ�A��B��C���ڵ��������ҵ��ʾ�Ϊ���壮��̬ʱ��A��Bԭ�Ӻ�����Ӿ��ɶԣ��Һ˵����A��B��ԭ�Ӱ뾶A��B��C��A�����ڱ�����ͬһ����Ԫ�أ�ԭ�Ӱ뾶�ӽ�����ͼ�ǽ���B��C���γɵ�ij�ֺϽ�ľ����ṹʾ��ͼ��D��E��F�����ڱ�������ͬһ����Dԭ���ڻ�̬ʱp���������ҵ縺����ͬ��Ԫ�������ģ�E������������������ͻԾ��Eԭ�ӵĵ�һ�����������ĵ����ܣ�kJ/mol���ֱ�Ϊ��578��1817��2745��11575��Fԭ���������ܲ㣬E��F���γ�ԭ����Ŀ��Ϊ1��3���۵�Ϊ190��Ļ�����Q����ش�
A��B��C��D��E��F����Ԫ�أ�A��B��C���ڵ��������ҵ��ʾ�Ϊ���壮��̬ʱ��A��Bԭ�Ӻ�����Ӿ��ɶԣ��Һ˵����A��B��ԭ�Ӱ뾶A��B��C��A�����ڱ�����ͬһ����Ԫ�أ�ԭ�Ӱ뾶�ӽ�����ͼ�ǽ���B��C���γɵ�ij�ֺϽ�ľ����ṹʾ��ͼ��D��E��F�����ڱ�������ͬһ����Dԭ���ڻ�̬ʱp���������ҵ縺����ͬ��Ԫ�������ģ�E������������������ͻԾ��Eԭ�ӵĵ�һ�����������ĵ����ܣ�kJ/mol���ֱ�Ϊ��578��1817��2745��11575��Fԭ���������ܲ㣬E��F���γ�ԭ����Ŀ��Ϊ1��3���۵�Ϊ190��Ļ�����Q����ش�| 1 |
| 6 |
| 1 |
| 2 |
| 1 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��32 g O2������ԭ����ĿΪNA |
| B��0.5 mol H2O����NA����ԭ�Ӻ�0.5NA����ԭ�� |
| C��1 mol H2O���е�H2O������ĿΪNA |
| D��0.5NA���������ӵ����ʵ�����0.5 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | Ԥ�������� | |
| ����1 | ȡ������ɫ��Һ������NaOH��Һ | ������ɺ��ɫ��������˵�������˷�Ӧ |
| ����2 | ȡ������ɫ��Һ��������۵⻯����Һ | �����Һ����ɫ����˵��δ������Ӧ |
| ����3 | ȡ������ɫ��Һ���������Ȼ�̼���� | ����²���Һ�ʳȺ�ɫ����˵���� |
| ʵ����� | Ԥ�������� | ������������ӷ���ʽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
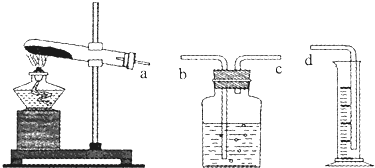
| ʵ�� ��� | KclO3��g�� | �������壨mL�� | ��ʱ ��s�� | |||
| ��ѧʽ | ������g�� | ʵ�ʻ��� | ||||
| 1 | 0.6 | - | - | - | 10 | 480 |
| 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.6 | Cr2O3 | 0.20 | �쳣 | 67.2 | 188.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ag+ |
| B��SO42- |
| C��SO42-��Ag+ |
| D��SO42-��Ag+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��̼��������ᷴӦ��CO32-+2H+=H2O+CO2�� |
| B��ϡH2SO4�����۷�Ӧ��Fe+4H+=Fe3++2H2�� |
| C������������Һ��ϡH2SO4��Ӧ��Ba2++SO42-=BaSO4�� |
| D��������������ϡ�����ϣ�Fe2O3+6H+=Fe3++3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com