
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | |||
| 4 | �� | �� |
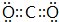 ���ʴ�Ϊ��C��Ar��
���ʴ�Ϊ��C��Ar��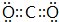 ��
�� ��
�� ��
��

 53���ò�ϵ�д�
53���ò�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NaCl |
| B��K2SO4 |
| C��CuCl2 |
| D��MgCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����£���25mL 0.1mol/L MOH��Һ����μ���0.2mol/L HA��Һ��������ͼ��ʾ������仯���Բ��ƣ�������˵��������ǣ�������
�����£���25mL 0.1mol/L MOH��Һ����μ���0.2mol/L HA��Һ��������ͼ��ʾ������仯���Բ��ƣ�������˵��������ǣ�������| A��MOH�ĵ��뷽��ʽΪMOH=M++OH- |
| B��MOH��HAǡ����ȫ��Ӧʱ����Һ�ʼ��ԣ�������A-+H2O=HA+OH-����ʱ�������Һ����ˮ�������c��H+������0.2mol/L HA��Һ����ˮ�������c��H+�� |
| C�������Һ����B�㣺c��M+��=c��A-����c��H+��=c��OH-������C�㣺c��A-����c��M+����c��H+����c��OH-�� |
| D����Һ��D��ʱ c��A-��+c��HA��=2c��M+��������ʱ���pH=3����c��HA��+c��H+��=0.05+10-11mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1����֪��C��s��+O2��g���TCO2��g����H=-393.5kJ/mol
��1����֪��C��s��+O2��g���TCO2��g����H=-393.5kJ/mol�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com