
 甲醇是一种重要的化工原料,有着重要的用途和应用前景.
甲醇是一种重要的化工原料,有着重要的用途和应用前景.分析 燃料电池的工作原理:电池的负极一定是燃料失电子,发生氧化反应,在正极上一定氧气得电子,发生还原反应,结合电极反应式判断溶液碱性变化,据此分析.
解答 解:①燃料电池的工作原理:通入甲醇的一极为负极,负极上甲醇失电子生成碳酸根离子,则负极的电极反应式为:CH3OH+8OH--6e-=CO32-+6H2O,通入氧气的一极为正极,正极上氧气得电子生成氢氧根离子,正极的电极反应式为:O2+2H2O+4e-=4OH-;电解质溶液中氢氧根离子向负极移动;
故答案为:正极;O2+2H2O+4e-=4OH-;CH3OH+8OH--6e-=CO32-+6H2O;负;
②在碱性环境下,甲醇反应生成的二氧化碳会消耗氢氧根离子,所以溶液的碱性减弱;
故答案为:减弱.
点评 本题考查原电池知识的应用,涉及电极判断与电极反应式书写等问题,做题时注意从氧化还原的角度判断原电池的正负极以及电极方程式的书写、注意溶液酸碱性对电极的影响,题目难度不大.


科目:高中化学 来源: 题型:选择题
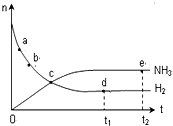 对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),在673K、30MPa下,n(NH3)和n(H2)随时间的变化关系如下图所示,下列说法正确的是( )
对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),在673K、30MPa下,n(NH3)和n(H2)随时间的变化关系如下图所示,下列说法正确的是( )| A. | 点a的正反应速率比点b的大 | |
| B. | 点c处反应达到平衡 | |
| C. | 点d (t1时刻)和点e (t2时刻)处n(N2)不一样 | |
| D. | 若开始充入1mol N2及足量H2,提供适当条件,可得2mol NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
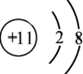
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水中既有分子,又有离子 | |
| B. | 久置的氯水可以使干燥的有色布条褪色 | |
| C. | 新制氯水中滴加硝酸银溶液,没有任何现象 | |
| D. | 新制氯水在光照条件下,可以产生气体,该气体是氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(4) | B. | (2)(4) | C. | (4) | D. | (3)(4)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
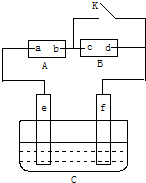 如图,A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
如图,A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是国际单位制中七个基本物理量之一 | |
| B. | Cl2的摩尔质量是71 g/mol | |
| C. | 标准状况下,22.4 L H2O的物质的量为1 mol | |
| D. | 1 mol H2的质量是1 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com