
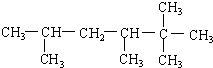 2,2,3,5-四甲基己烷
2,2,3,5-四甲基己烷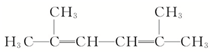 2,5-二甲基-2,4-己二烯.
2,5-二甲基-2,4-己二烯. 分析 烷烃的命名原则:碳链最长称某烷,靠近支链把号编.简单在前同相并,其间应划一短线;
烯烃的命名原则:选取含有碳碳双键的最长碳链为主链,选取距离双键最近的一端命名为1号碳.
解答 解:(1)(CH3)2CH(CH2)2CH(C2H5)(CH2)2CH3 的最长碳链为8,在2号碳上含有1个甲基,在5号碳上含有1个乙基,正确命名为:2-甲基-5-乙基辛烷,故答案为:2-甲基-5-乙基辛烷;
(2)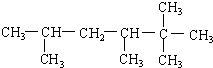 的最长碳链为6,从右端命名,在2号碳上含有2个甲基,在3和5号碳山河各含有1个甲基,正确命名为:2,2,3,5-四甲基己烷,故答案为:2,2,3,5-四甲基己烷;
的最长碳链为6,从右端命名,在2号碳上含有2个甲基,在3和5号碳山河各含有1个甲基,正确命名为:2,2,3,5-四甲基己烷,故答案为:2,2,3,5-四甲基己烷;
(3)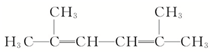 含有2个碳碳双键,为二烯烃,最长碳链为6,为对称结构,在2和5号碳上含有1个甲基,碳碳双键分别在2、3号碳和4、5号碳之间,正确命名为:2,5-二甲基-2,4-己二烯,故答案为:2,5-二甲基-2,4-己二烯.
含有2个碳碳双键,为二烯烃,最长碳链为6,为对称结构,在2和5号碳上含有1个甲基,碳碳双键分别在2、3号碳和4、5号碳之间,正确命名为:2,5-二甲基-2,4-己二烯,故答案为:2,5-二甲基-2,4-己二烯.
点评 本题考查了烷烃和烯烃的系统命名法,题目难度中等,可以根据“碳链最长称某烷,靠近支链把号编.简单在前同相并,其间应划一短线”进行命名.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | E | H | F | I | ||||
| 3 | A | C | D | G | R | |||
| 4 | B |
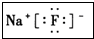 .并用电子式表示该化合物的形成过程_
.并用电子式表示该化合物的形成过程_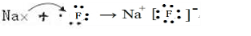
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 124 g P4含有P-P键的个数为4NA | |
| B. | 12 g石墨中含有C-C键的个数为1.5NA | |
| C. | 28 g晶体硅中含有Si-Si键的个数为4NA | |
| D. | 60 g SiO2中含Si-O键的个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-12 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取代,4 mol Cl2 | B. | 加成,2 mol Cl2 | ||
| C. | 加成、取代,2 mol Cl2 | D. | 加成、取代,3 mol Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1:6 | B. | 3:2:6 | C. | 1:2:5 | D. | 1:2:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 做有关硫的实验残留的硫 | B. | 做碘升华实验残留的碘 | ||
| C. | 用KMnO4制O2后留下的固体 | D. | 沾有AgCl沉淀的试管 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com