
ĻĀĮŠĪļÖŹÖŠ£¬¼Čŗ¬ÓŠĄė×Ó¼üÓÖŗ¬ÓŠ¼«ŠŌ¹²¼Ū¼üµÄŹĒ£Ø £©
A£®Na2O2 B£®MgCl2 C£®HCl D£®NH4Cl
 æĘѧŹµŃé»ī¶Æ²įĻµĮŠ“š°ø
æĘѧŹµŃé»ī¶Æ²įĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014øßæ¼»Æѧ×ØĢāĶ»ĘĘѵĮ· ×ØĢā13ĪļÖŹ½į¹¹ÓėŠŌÖŹŃ”ŠŽ3Į·Ļ°¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
A”¢B”¢C”¢DŹĒŌŖĖŲÖÜĘŚ±ķÖŠĒ°36ŗÅŌŖĖŲ,ĖüĆĒµÄŗĖµēŗÉŹżŅĄ“ĪŌö“ó”£AŌ×ÓL²ćµÄ³É¶Ōµē×ÓŹżŗĶĪ“³É¶Ōµē×ÓŹżĻąµČ,BŌ×ÓµÄ×īĶā²ćp¹ģµĄµÄµē×ÓĪŖ°ė³äĀś½į¹¹,CŹĒµŲæĒÖŠŗ¬Įæ×ī¶ąµÄŌŖĖŲ”£DŹĒµŚĖÄÖÜĘŚŌŖĖŲ,ĘäŌ×ÓŗĖĶā×īĶā²ćµē×ÓŹżÓėĒāŌ×ÓĻąĶ¬,ĘäÓąø÷²ćµē×Ó¾ł³äĀś”£Ēė»Ų“šĻĀĮŠĪŹĢā:
(1)A”¢B”¢CµÄµŚŅ»µēĄėÄÜÓÉŠ”µ½“óµÄĖ³ŠņŹĒ (ÓƶŌÓ¦µÄŌŖĖŲ·ūŗűķŹ¾);»łĢ¬DŌ×ӵĵē×ÓÅŲ¼Ź½ĪŖ ”£
(2)AµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ·Ö×ÓÖŠ,ĘäÖŠŠÄŌ×Ó²ÉČ” ŌÓ»Æ;B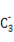 µÄæռ乹ŠĶĪŖ (ÓĆĪÄ×ÖĆčŹö)”£
µÄæռ乹ŠĶĪŖ (ÓĆĪÄ×ÖĆčŹö)”£
(3)1 mol AB-ÖŠŗ¬ÓŠµÄ¦Š¼üøöŹżĪŖ ”£
(4)ČēĶ¼ŹĒ½šŹōCaŗĶDĖłŠĪ³ÉµÄijÖÖŗĻ½šµÄ¾§°ū½į¹¹Ź¾ŅāĶ¼,ŌņøĆŗĻ½šÖŠCaŗĶDµÄŌ×ÓøöŹż±ČŹĒ ”£
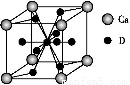
(5)ļēÄųŗĻ½šÓėÉĻŹöŗĻ½š¶¼¾ßÓŠĻąĶ¬ĄąŠĶµÄ¾§°ū½į¹¹XYn,ĖüĆĒÓŠŗÜĒæµÄ“¢ĒāÄÜĮ¦”£ŅŃÖŖļēÄųŗĻ½šLaNin¾§°ūĢå»żĪŖ9.0”Į10-23 cm3,“¢ĒāŗóŠĪ³ÉLaNinH4.5ŗĻ½š(Ēā½ųČė¾§°ūæÕĻ¶,Ģå»ż²»±ä),ŌņLaNinÖŠn= (ĢīŹżÖµ);ĒāŌŚŗĻ½šÖŠµÄĆܶČĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014½ĖÕŹ”ŃļÖŻŹŠ½ģøßČżÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
¶ž¼×ĆŃ£ØDME£©±»ÓžĪŖ”°21ŹĄ¼ĶµÄĒå½ąČ¼ĮĻ”±”£ÓÉŗĻ³ÉĘųÖʱø¶ž¼×ĆѵÄÖ÷ŅŖŌĄķČēĻĀ£ŗ
¢Ł CO(g)+2H2(g)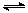 CH3OH(g) ”÷H 1=£90.7 kJ”¤mol-1
CH3OH(g) ”÷H 1=£90.7 kJ”¤mol-1
¢Ś 2CH3OH(g)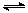 CH3OCH3(g)+H2O(g) ”÷H 2=£23.5 kJ”¤mol-1
CH3OCH3(g)+H2O(g) ”÷H 2=£23.5 kJ”¤mol-1
¢Ū CO(g)+H2O(g)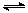 CO2(g)+H2(g) ”÷H 3=£41.2kJ”¤mol-1
CO2(g)+H2(g) ”÷H 3=£41.2kJ”¤mol-1
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ōņ·“Ó¦3H2(g)£«3CO(g)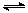 CH3OCH3(g)£«CO2(g)µÄ”÷H£½ kJ”¤mol-1”£
CH3OCH3(g)£«CO2(g)µÄ”÷H£½ kJ”¤mol-1”£
£Ø2£©ĻĀĮŠ“ėŹ©ÖŠ£¬ÄÜĢįøßCH3OCH3²śĀŹµÄÓŠ ”£
A£®Ź¹ÓĆ¹żĮæµÄCO B£®ÉżøßĪĀ¶Č C£®Ōö“óŃ¹Ēæ
£Ø3£©·“Ó¦¢ŪÄÜĢįøßCH3OCH3µÄ²śĀŹ£¬ŌŅņŹĒ ”£
£Ø4£©½«ŗĻ³ÉĘųŅŌn(H2)/n(CO)=2ĶØČė1 LµÄ·“Ó¦Ę÷ÖŠ£¬Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗ
4H2(g)+2CO(g) 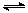 CH3OCH3(g)+H2O(g) ”÷H£¬ĘäCOµÄĘ½ŗā×Ŗ»ÆĀŹĖęĪĀ¶Č”¢Ń¹Ēæ±ä»Æ¹ŲĻµČēĶ¼1ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ”£
CH3OCH3(g)+H2O(g) ”÷H£¬ĘäCOµÄĘ½ŗā×Ŗ»ÆĀŹĖęĪĀ¶Č”¢Ń¹Ēæ±ä»Æ¹ŲĻµČēĶ¼1ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ”£
A£®”÷H <0
B£®P1<P2<P3
C£®ČōŌŚP3ŗĶ316”ꏱ£¬ĘšŹ¼Ź±n(H2)/n(CO)=3£¬Ōņ“ļµ½Ę½ŗāŹ±£¬CO×Ŗ»ÆĀŹŠ”ÓŚ50£„[
£Ø5£©²ÉÓĆŅ»ÖÖŠĀŠĶµÄ“߻ƼĮ£ØÖ÷ŅŖ³É·ÖŹĒCu-MnµÄŗĻ½š£©£¬ĄūÓĆCOŗĶH2Öʱø¶ž¼×ĆŃ”£¹Ū²ģĶ¼2»Ų“šĪŹĢā”£“߻ƼĮÖŠn(Mn)/n(Cu)Ō¼ĪŖ Ź±×īÓŠĄūÓŚ¶ž¼×ĆѵÄŗĻ³É”£
£Ø6£©Ķ¼3ĪŖĀĢÉ«µēŌ“”°¶ž¼×ĆŃČ¼ĮĻµē³Ų”±µÄ¹¤×÷ŌĄķŹ¾ŅāĶ¼£¬aµē¼«µÄµē¼«·“Ó¦Ź½ĪŖ ”£
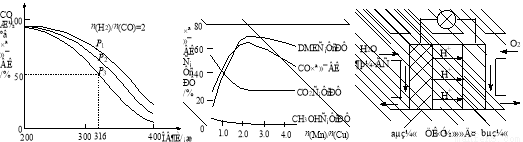
Ķ¼1 Ķ¼2 Ķ¼3
£Ø7£©¼×“¼ŅŗĻąĶŃĖ®·ØÖʶž¼×ĆѵÄŌĄķŹĒ£ŗCH3OH +H2SO4”śCH3HSO4+H2O£¬
CH3 HSO4+CH3OH”śCH3OCH3+H2SO4”£ÓėŗĻ³ÉĘųÖʱø¶ž¼×ĆŃ±Č½Ļ£¬øĆ¹¤ŅÕµÄÓŵćŹĒ·“Ó¦ĪĀ¶ČµĶ£¬×Ŗ»ÆĀŹøߣ¬ĘäȱµćŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014½ĖÕŹ”ŃļÖŻŹŠ½ģøßČżÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
³£ĪĀĻĀ£¬ĻĀĮŠø÷×éĄė×ÓŌŚÖø¶ØČÜŅŗÖŠŅ»¶ØÄÜ“óĮæ¹²“ęµÄŹĒ
A£®0.1 mol”¤L-1µÄKIČÜŅŗ£ŗ Na£«”¢Ag+”¢NO3-”¢SO42-
B£®Ź¹¼×»ł³Č±äŗģÉ«µÄČÜŅŗ£ŗNH4+”¢Cu2+”¢ClO£”¢Cl£
C£®0.1 mol”¤L-1µÄKMnO4ČÜŅŗ£ŗNa£«”¢K£«”¢Cl£”¢SO32-
D£®Óö±½·Ó±ä×ĻÉ«µÄČÜŅŗ£ŗNa£«”¢Mg2+”¢SO42-”¢Cl£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014Äźøßæ¼»ÆѧĖÕ½Ģ°ę×Üø“Ļ°5-3Ī¢Į£¼äĻą»„×÷ÓĆĮ¦ÓėĪļÖŹ¶ąŃłŠŌĮ·Ļ°¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĪļÖŹÓėĘäĖłŗ¬»Æѧ¼üĄąŠĶ”¢ĖłŹō»ÆŗĻĪļĄąŠĶĶźČ«ÕżČ·µÄŅ»×éŹĒ£Ø £©
A£®CO2”¢¹²¼Ū¼ü”¢¹²¼Ū»ÆŗĻĪļ
B£®MgCl2”¢Ąė×Ó¼üŗĶ¹²¼Ū¼ü”¢Ąė×Ó»ÆŗĻĪļ
C£®H2O”¢Ąė×Ó¼ü”¢¹²¼Ū»ÆŗĻĪļ
D£®NaOH”¢Ąė×Ó¼üŗĶ¹²¼Ū¼ü”¢¹²¼Ū»ÆŗĻĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014Äźøßæ¼»ÆѧĖÕ½Ģ°ę×Üø“Ļ°5-3Ī¢Į£¼äĻą»„×÷ÓĆĮ¦ÓėĪļÖŹ¶ąŃłŠŌĮ·Ļ°¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
½«µČĪļÖŹµÄĮæµÄĮņĖįŗĶĒāŃõ»ÆÄĘ·“Ó¦ŗóĖłµĆµ½µÄČÜŅŗÕōøÉ£¬æɵƵ½NaHSO4”£ĻĀĮŠ¹ŲÓŚNaHSO4µÄĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©
A£®ŅņĪŖNaHSO4ŹĒĄė×Ó»ÆŗĻĪļ£¬Ņņ“ĖÄܹ»µ¼µē
B£®NaHSO4¹ĢĢåÖŠŃōĄė×ÓŗĶŅõĄė×ÓµÄøöŹż±ČŹĒ2£ŗ1
C£®NaHSO4¹ĢĢåČŪ»ÆŹ±ĘĘ»µµÄŹĒĄė×Ó¼üŗĶ¹²¼Ū¼ü
D£®NaHSO4¹ĢĢåČÜÓŚĖ®Ź±¼ČĘĘ»µĄė×Ó¼üÓÖĘĘ»µ¹²¼Ū¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014Äźøßæ¼»ÆѧĖÕ½Ģ°ę×Üø“Ļ°10-1»ÆѧŹµŃé³£ÓĆŅĒĘ÷ŗĶ»ł±¾²Ł×÷Į·Ļ°¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃé²Ł×÷ÕżČ·µÄŹĒ( )
¢ŁÓĆ50 mLĮæĶ²ĮæČ”5.2 mLĻ”ĮņĖį£»¢ŚÓĆ·ÖŅŗĀ©¶··ÖĄė±½ŗĶĖÄĀČ»ÆĢ¼µÄ»ģŗĻĪļ£»¢ŪÓĆĶŠÅĢĢģĘ½³ĘĮæ117.7 gĀČ»ÆÄĘ¾§Ģ壻¢ÜÓĆ¼īŹ½µĪ¶Ø¹ÜĮæČ”23.10 mLäåĖ®£»¢ŻÓĆ“ÉŪįŪö×ĘÉÕø÷ÖÖÄʵĻÆŗĻĪļ£»¢ŽÓĆ250 mLČŻĮæĘæÅäÖĘ250 mL 0.2 mol”¤L£1µÄNaOHČÜŅŗ£»¢ßÓĆÅØŃĪĖįĒåĻ“×ö¹żKMnO4·Ö½āŹµŃéµÄŹŌ¹Ü£»¢ą½«ÅØĻõĖį±£“ęŌŚĪŽÉ«ŹŌ¼ĮĘæÖŠ”£
A£®¢Ł¢Ś¢Ü B£®¢Ś¢Ū¢Ü¢Ż C£®¢Ū¢Ž¢ß D£®¢Ś¢Ż¢Ž¢ą
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014Äźøßæ¼»ÆѧĖÕ½Ģ°ę×Üø“Ļ° 9-3 ČĖ¹¤ŗĻ³ÉÓŠ»ś»ÆŗĻĪļĮ·Ļ°¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ij·Ö×ÓŹ½ĪŖC10H20O2µÄõ„£¬ŌŚŅ»¶ØĢõ¼žĻĀæÉ·¢ÉśČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ż³Ģ£ŗ
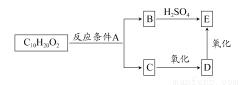
Ōņ·ūŗĻÉĻŹöĢõ¼žµÄõ„µÄ½į¹¹æÉÓŠ( )
A£®2ÖÖ B£®4ÖÖ C£®6ÖÖ D£®8ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014Äźøßæ¼»ÆѧĖÕ½Ģ°ę×Üø“Ļ° 8-4 ÄŃČܵē½āÖŹµÄČܽāĘ½ŗāĮ·Ļ°¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
(1)ŌŚ“ÖÖĘCuSO4”¤5H2O¾§ĢåÖŠ³£ŗ¬ÓŠŌÓÖŹFe2£«”£ŌŚĢį“æŹ±ĪŖĮĖ³żČ„Fe2£«£¬³£¼ÓČėŗĻŹŹµÄŃõ»Æ¼Į£¬Ź¹Fe2£«±»Ńõ»ÆĪŖFe3£«£¬ĻĀĮŠĪļÖŹæɲÉÓƵďĒ________”£
A£®KMnO4””””B£®H2O2””””C£®ĀČĖ®””””D£®HNO3
Č»ŗóŌŁ¼ÓČėŹŹµ±ĪļÖŹµ÷ÕūÖĮČÜŅŗpH£½4£¬Ź¹Fe3£«×Ŗ»ÆĪŖFe(OH)3£¬æÉŅŌ“ļµ½³żČ„Fe3£«¶ų²»ĖšŹ§CuSO4µÄÄæµÄ£¬µ÷ÕūČÜŅŗpHæÉŃ”ÓĆĻĀĮŠÖŠµÄ________”£
A£®NaOH B£®KOH C£®CuO D£®Cu(OH)2
(2)¼×Ķ¬Ń§»³Ņɵ÷ÕūÖĮČÜŅŗpH£½4²»Ņ»¶ØÄÜ“ļµ½³żČ„Fe3£«¶ų²»ĖšŹ§Cu2£«µÄÄæµÄ”£ŅŅĶ¬Ń§ČĻĪŖæÉŅŌĶعż¼ĘĖćČ·¶Ø£¬Ėū²éŌÄÓŠ¹Ų׏ĮĻµĆµ½ČēĻĀŹż¾Ż£¬³£ĪĀĻĀFe(OH)3µÄČܶȻżKsp£½8.0”Į10£38£¬Cu(OH)2µÄČܶȻżKsp£½3.0”Į10£20£¬Ķس£²ŠĮōŌŚČÜŅŗÖŠµÄĄė×ÓÅØ¶ČŠ”ÓŚ1”Į10£5mol”¤L£1Ź±¾ĶČĻĪŖ³ĮµķĶźČ«£¬ÉčČÜŅŗÖŠCuSO4µÄÅضČĪŖ3.0 mol”¤L£1£¬ŌņCu(OH)2æŖŹ¼³ĮµķŹ±ČÜŅŗµÄpHĪŖ________£¬Fe3£«ĶźČ«³ĮµķŹ±ČÜŅŗµÄpHĪŖ________£¬Ķعż¼ĘĖćČ·¶ØÉĻŹö·½°ø________”£(Ģī”°æÉŠŠ”±»ņ”°²»æÉŠŠ”±)”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com