
| A. | x+y<z | B. | 平衡逆向移动 | C. | A的转化率降低 | D. | C的体积分数升高 |
分析 平衡时测得A的浓度为0.5mol?L-1,保持温度不变,将容器的容积缩小到原来的一半,如平衡不移动,则A的浓度应为1mol/L,而此时为0.9mol/L,则说明增大压强平衡向正方向移动,以此进行判断.
解答 解:平衡时测得A的浓度为0.5mol?L-1,保持温度不变,将容器的容积缩小到原来的一半,如平衡不移动,则A的浓度应为1mol/L,而此时为0.9mol/L,则说明增大压强平衡向正方向移动,
A.增大压强平衡向正方向移动,说明反应物气体的计量数之和大于生成物气体的计量数,应为x+y>z,故A错误;
B.由以上分析可知平衡向正方向移动,故B错误;
C.平衡向正方向移动,A的转化率增大,故C错误;
D.平衡向正方向移动,C的体积分数增大,故D正确.
故选D.
点评 本题考查化学平衡移动知识,题目难度不大,注意从浓度的变化的角度判断平衡移动的方向,结合压强对平衡移动的影响分析.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ② | C. | ③ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 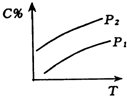 | B. | 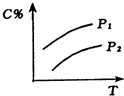 | C. | 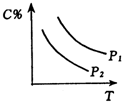 | D. | 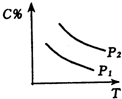 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨基酸、淀粉均属于高分子化合物 | |
| B. | 乙醇不能发生取代反应 | |
| C. | 苯能使溴水褪色是因为发生了加成反应 | |
| D. | 乙烯和甲烷可用溴的四氯化碳溶液鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4中混有C2H4,可通过KMnO4酸性溶液除去CH4中C2H4 | |
| B. | 苯与液溴在铁粉催化下反应生成有苦杏仁味的溴苯 | |
| C. | 除去乙醇中的水可先加生石灰,再蒸馏 | |
| D. | 己烷与苯的混合溶液可用分液法分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某小组设计如图装置(盐桥中盛有浸泡了KNO3溶液的琼脂)研究电化学原理.请完成下列问题:
某小组设计如图装置(盐桥中盛有浸泡了KNO3溶液的琼脂)研究电化学原理.请完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何可逆反应都有一定的限度 | |
| B. | 对于反应2SO2(g)+O2(g)?2SO3(g)只有达到限度时才有2v(O2)=v(SO3) | |
| C. | 对于反应2SO2(g)+O2(g)?2SO3(g)达到限度时,增大容器容积能减小正反应速率 | |
| D. | 化学反应达到限度时,正逆反应速率相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com