
| A. | c(H+)=1×10-14mol/L的无色溶液:K+、S2-、MnO4-、SO42- | |
| B. | 水电离出的c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32- | |
| C. | 能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I- | |
| D. | 能使甲基橙变红的溶液中:Na+、NH4+、Fe2+、NO3- |
分析 A.有颜色的离子不能大量存在;
B.水电离出的c(H+)=1×10-14mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性;
C.能与Al反应产生H2的溶液可以为酸性和碱性溶液;
D.能使甲基橙变红的溶液呈酸性.
解答 解:A.无色溶液,MnO4-为紫色,故A错误;
B.水电离出的c(H+)=1×10-14mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,碱性条件下,离子之间不发生任何反应,可大量共存,故B正确;
C.能与Al反应产生H2的溶液可以为酸性和碱性溶液,但酸性溶液中NO3-和I-不能共存,且不生成氢气,能发生氧化还原反应,碱性溶液中NH4+要与OH-反应产生氨气,故C错误;
D.能使甲基橙变红的溶液呈酸性,NO3-和Fe2+不能共存,要发生氧化还原反应,故D错误.
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
 控制适合的条件,将反应AsO43-+2I-+2H+? AsO33-+I2+H2O 设计成如图所示的原电池.下列判断正确的是( )
控制适合的条件,将反应AsO43-+2I-+2H+? AsO33-+I2+H2O 设计成如图所示的原电池.下列判断正确的是( )| A. | 反应开始时,B池中石墨电极上发生氧化反应 | |
| B. | 反应开始时,A池中石墨电极上I-被还原 | |
| C. | 反应开始时,盐桥中K+由左向右迁移 | |
| D. | 电流计读数为零后,在B池中溶入Na3AsO3固体,B池中的石墨电极为正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2[PtCl2(OH)4]具有很强的碱性 | B. | 3种含铂化合物的配位数均为6 | ||
| C. | 3种含铂化合物都属于共价化合物 | D. | 3种含铂配合物中Pt的化合价不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L氯气溶于水转移电子数为NA | |
| B. | 1L 0.1mol/L的硫酸铁溶液中含有铁离子的数目为0.2NA | |
| C. | 向氨气合成塔中通入amolN2和3amolH2的混合气,充分反应后生成N-H数为6aNA | |
| D. | 电解硫酸铜溶液时,当阳极产生22.4L(标况)气体,体系中转移电子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由H、N、O三种元素形成的化合物中一定含有共价键 | |
| B. | 正戊烷、异丁烷和丙烷属于同系物,沸点依次升高 | |
| C. | 葡萄糖能发生银镜反应,蔗糖、麦芽糖也能发生银镜反应 | |
| D. | 用KSCN溶液检验Fe3+的实验现象是产生血红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
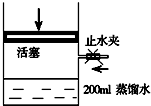 有A、B、C、D、E五种短周期元素,A、C同周期,B、D同主族,E是五种元素中原子半径最小的元素.A是构成矿物和岩石的主要成分的元素,C、D可生成离子化合物C3D2.A的单质与E的单质在常温下就可发生反应,生成化合物F.据此回答下列问题:
有A、B、C、D、E五种短周期元素,A、C同周期,B、D同主族,E是五种元素中原子半径最小的元素.A是构成矿物和岩石的主要成分的元素,C、D可生成离子化合物C3D2.A的单质与E的单质在常温下就可发生反应,生成化合物F.据此回答下列问题: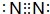 ;A单质及其最高价氧化物均属于原子晶体(填晶体类型)
;A单质及其最高价氧化物均属于原子晶体(填晶体类型)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
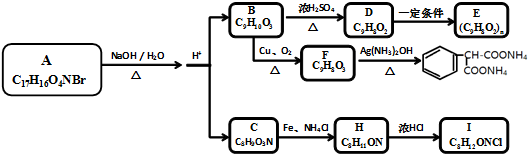
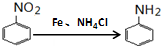
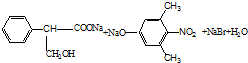
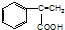 ,C→H的反应类型是还原反应.
,C→H的反应类型是还原反应.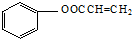 ,
,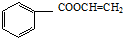 .
.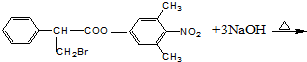
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
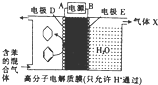 一定条件下,利用如图所示装置可实现有机物的储氢,下列有关说法正确的是( )
一定条件下,利用如图所示装置可实现有机物的储氢,下列有关说法正确的是( )| A. | A为电源的正极 | |
| B. | 气体X为H2 | |
| C. | 电极E为阴极 | |
| D. | 电极D的电极反应式为C6H6+6H++6e-=C6H12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知A-+H2B(过量)=HA+HB-,则结合H+的能力:HB-<A-<B2- | |
| B. | 在25℃时,将cmol/L的醋酸溶液与0.02mol/LNaOH溶液等体积混合后溶液恰好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=2×10-9/(c-0.02) | |
| C. | 若将CO2 通入0.1 mol/LNaOH溶液中至溶液中性,则溶液中2 c(CO32ˉ)+c(HCO3ˉ)=0.1 mol/L | |
| D. | 常温下,将相同体积的pH=3硫酸和pH=11一元碱BOH溶液混合,所得溶液可能为中性也可能为碱性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com