
| A. | 1mol任何气体的气体摩尔体积都约为22.4L/mol | |
| B. | 常温常压下,11.2LO3中所含氧原子个数等于1.5NA | |
| C. | 标准状况下,1mol CCl4所占的体积约为22.4L | |
| D. | 同温、同压下,相同体积的一氧化碳和二氧化碳的质量比为7:11 |
分析 A.气体摩尔体积与温度和压强有关;
B.常温常压下,气体摩尔体积大于22.4L/mol;
C.标况下四氯化碳是液体,气体摩尔体积对其不适用;
D.同温同压下,气体摩尔体积相同,相同体积的二氧化碳和CO其物质的量相同,根据m=nM计算其质量之比.
解答 解:A.气体摩尔体积与温度和压强有关,温度和压强未知所以其气体摩尔体积未知,故A错误;
B.常温常压下,气体摩尔体积大于22.4L/mol,则11.2LO3的物质的量小于0.5mol,则所含氧原子个数小于1.5NA,故B错误;
C.标况下四氯化碳是液体,气体摩尔体积对其不适用,所以无法计算四氯化碳体积,故C错误;
D.同温同压下,气体摩尔体积相同,相同体积的二氧化碳和CO其物质的量相同,根据m=nM知,其质量与摩尔质量成正比,其质量之比=28g/mol:44g/mol=7:11,故D正确;
故选D.
点评 本题考查物质的量有关计算,为高频考点,明确物质的量公式中各个物理量关系是解本题关键,注意气体摩尔体积适用范围及其适用条件,题目难度不大,易错选项是C.


科目:高中化学 来源: 题型:解答题
| 实验 编号 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 /mL | ||
| 体积/mL | 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | |||
| ① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
| ② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| ③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
| ④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
| ⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上F单质用MnO2和AF来制备 | |
| B. | B元素所形成的单质的晶体类型都是相同的 | |
| C. | F所形成的氢化物的酸性强于BD2的水化物的酸性,说明F的非金属性强于B | |
| D. | 由化学键角度推断,能形成BDF2这种化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
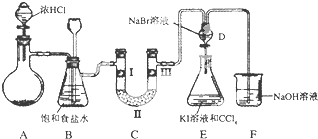
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 碱石灰 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铜溶液与氢氧化钡溶液混合:Ba2++SO42-═BaSO4↓ | |
| B. | 澄清的石灰水与稀盐酸反应:OH-+H+═H2O | |
| C. | 硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-═AgCl↓+NO3- | |
| D. | 铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①>② | B. | ①<② | C. | ①=② | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Cu2+、NO3-、SO42- | B. | K+、H+、SO42-、OH- | ||
| C. | Al3+、NH4+、OH-、Cl- | D. | Ca2+、Na+、Cl-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酸性KMnO4溶液将Fe2+氧化成Fe3+,再转化为Fe(OH)3沉淀除去 | |
| B. | 用ZnO调节浸出液的酸碱性,可使某些离子形成氢氧化物沉淀 | |
| C. | 在实际生产过程中,加入Ag2SO4可除去Cl-,是利用了沉淀转化的原理 | |
| D. | 也可以用ZnCO3代替ZnO调节溶液的酸碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用电泳现象区别溶液和胶体 | |
| B. | 用渗析的方法除去胶体中的离子或分子,以净化胶体 | |
| C. | 用滤纸过滤除去溶液中的胶体粒子 | |
| D. | 向新制Fe(OH)3胶体中加入足量AgNO3溶液,以除去胶体中的Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com