
| A. | 2Al2O3(熔融) $\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑ | |
| B. | Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | |
| C. | Fe+CuSO4=FeSO4+Cu | |
| D. | 2NaCl(水溶液)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑ |
分析 金属冶炼是工业上将金属从含有金属元素的矿石中还原出来的生产过程.金属的活动性不同,可以采用不同的冶炼方法.
金属冶炼的方法主要有:
热分解法:对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来(Hg及后边金属);
热还原法:在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来(Zn~Cu);
合电解法:活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属(K~Al).
解答 解:A、铝很活泼,加入冰晶石降低氧化铝的熔点,工业上电解熔融氧化铝冶炼铝,故A正确;
B、铁位于金属活动顺序表中间位置的金属,通常用热还原法冶炼,故B正确;
C、铁比铜活泼,能从铜的盐溶液中置换出铜,故C正确;
D、氢离子的氧化性比钠离子强,在溶液中电解,氢离子放电,钠离子不放电,电解NaCl水溶液得不到金属Na,故D错误.
故选D.
点评 本题考查了金属冶炼的一般原理,难度不大,注意根据金属的活泼性不同采取相应的冶炼方法.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 一定有乙烯 | B. | 一定有甲烷 | C. | 一定没有甲烷 | D. | 可能有乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯分子中C原子均以sp3杂化方式成键,形成夹角为120°的三个sp3杂化轨道,故为正六边形的碳环 | |
| B. | 每个碳原子还有一个未参与杂化的2p轨道,垂直碳环平面,相互交盖,形成大π键 | |
| C. | 大π键中6个电子被6个C原子共用,故称为6中心6电子大π键 | |
| D. | 苯分子中共有十二个原子共面,六个碳碳键完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其它 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、苯都不能发生氧化反应 | |
| B. | 乙烯、聚乙烯都可与溴水发生加成反应 | |
| C. | 一氯丙烷(C3H7Cl)的同分异构体共有3种 | |
| D. | 乙酸乙酯、油脂与NaOH溶液反应均有醇类物质生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
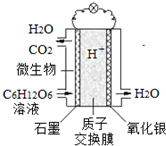 最近科学家研制的一种新型“微生物电池”可以将污水中的有机物转化为电能,其原理示意如图.下列有关该电池的说法正确的是( )
最近科学家研制的一种新型“微生物电池”可以将污水中的有机物转化为电能,其原理示意如图.下列有关该电池的说法正确的是( )| A. | 电池工作时,H+向石墨电极移动 | |
| B. | 石墨电极上反应为:C6H12O6+6H2O-24e-=6CO2↑+24H+ | |
| C. | 氧化银电极上反应为:Ag2O+2e-=2Ag+O2- | |
| D. | 该电池每转移4mol电子,石墨电极产生33.6 L CO2气体(标准状况) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液与稀硫酸的反应:OH-+H++Ba2++SO42-=BaSO4↓+H2O | |
| B. | 硫酸铝溶液中加入过量氨水:Al3++4OH-═[Al(OH)4]- | |
| C. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ | |
| D. | 碳酸钙溶于稀盐酸中:CO32-+2H+=H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯、乙醇和乙酸都能发生取代反应 | |
| B. | 液化石油气和天然气的主要成分都是甲烷 | |
| C. | 油脂在碱的催化作用下可发生水解,工业上利用该反应生产肥皂 | |
| D. | 用新制的Cu(OH)2悬浊液可检验尿液中的葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=c(CH3COO-)+c(OH-) | B. | c (Na+)>c (CH3COO-)>c(OH-)>c(H+) | ||
| C. | c(Na+)=c(CH3COO-)>c(OH-)=c(H+) | D. | c (CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com