
| A. | 摩尔既是物质的量的单位又是物质的质量单位 | |
| B. | 物质的量既表示物质的数量又表示物质的质量 | |
| C. | 阿伏加德罗常数是12kg碳12中含有的碳原子数目 | |
| D. | 1molH2O中含有10mol电子 |
分析 A.摩尔是物质的量的单位;
B.物质的量是一个物理量,不表示质量;
C.1mol任何粒子的粒子数叫做阿伏伽德罗常数;
D.分子中电子数等于质子数.
解答 解:A.摩尔是物质的量的单位,不是物质的质量的单位,故A错误;
B.物质的量是一个物理量,是一定数目粒子的几何体,不表示质量,故B错误;
C.1mol任何粒子的粒子数叫做阿伏伽德罗常数,1mol任何粒子的粒子数与0.012kg 12C中含有的碳原子数目相同,故C错误;
D.1molH2O中含有电子数=1×2+8=10mol,故D正确.
故选D.
点评 本题考查了物质的量及其单位、气体摩尔体积,题目难度不大,侧重于基础知识的考查,注意核电荷数=质子数=电子数=原子序数.


科目:高中化学 来源: 题型:解答题
 铊的相关信息卡片如图所示:
铊的相关信息卡片如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;D若为纯净物,D的核磁共振氢谱存在2种吸收峰,面积比为1:1;
;D若为纯净物,D的核磁共振氢谱存在2种吸收峰,面积比为1:1; ,反应类型:消去反应;
,反应类型:消去反应;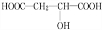 +HCOOH$?_{△}^{浓硫酸}$
+HCOOH$?_{△}^{浓硫酸}$ +H2O,反应类型:取代反应;
+H2O,反应类型:取代反应; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出 | |
| B. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| C. | 蒸馏操作时,应向蒸馏烧瓶中加入几块沸石,以防止暴沸 | |
| D. | 萃取操作时,可以选用CCl4或酒精作为萃取剂从溴水中萃取溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属氧化物一定是碱性氧化物 | |
| B. | 胶体和其他分散系的本质区别是分散质粒子大小不同 | |
| C. | 生石灰、醋酸、纯碱、氯化钠对应的物质类别是氧化物、酸、碱、盐 | |
| D. | 酸性氧化物一定是非金属氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 240 mL 0.2 mol•L-1的NaOH溶液配制:需要使用天平、烧杯、250 mL容量瓶等仪器 | |
| B. | 除去Cu粉中的CuO,可向混合物中滴加适量稀硫酸再过滤 | |
| C. | 为增强氯水的漂白性,向其中加入碳酸钙 | |
| D. | 为使0.5mol/L的NaNO3溶液物质的量浓度变为1mol/L,可将原溶液加热蒸发掉50克水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三氯化铁溶液中加入铁粉:Fe3++Fe═2Fe2+ | |
| B. | 苯酚钠溶液中通入少量CO2:CO2+H2O+C6H5O-→C6H5OH+HCO3- | |
| C. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | 用浓盐酸与MnO2反应制取少量氯气:MnO2+4H++4Cl-═Mn2++Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgSO4 溶液与Ba(OH)2溶液反应:SO42-+Ba2+═Ba SO4↓ | |
| B. | 钠与水的反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| C. | 铝片与氢氧化钠溶液反应:2Al+2OH--+2H2O═AlO2-+3H2↑ | |
| D. | 氢氧化铁溶于氢碘酸中Fe(OH)3+3H+═Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com