
����Ŀ��������Ϊʲô������������������Ľṹ�й�(��ͼ)�������й�˵���������

A.��������Ĵ��ڣ�ˮ���ӵ��ȶ��Ժã�������Ҳ���ѷֽ�
B.��һ���̬���У�ˮ���Ӽ�ͨ������γɿռ���״�ṹ
C.�ڶ�����Һ�����У�ˮ���Ӽ��γ�����Ļ���ȹ�̬������
D.������һ���¶�ʱ����Һ�����е�ˮ�������²�����ӵ�������ѣ������������Ե�ˮ��������ʹ����们
���𰸡�A
��������
A��ˮ���ӵ��ȶ��Ժã�����ˮ�������������ۼ��ļ��ܾ����ģ�����Ӽ��γɵ�����أ�A����
B����̬���У�1��ˮ��������Χ��4��ˮ����ͨ����������ӣ��Ӷ��γɿռ���״�ṹ��B��ȷ��
C����Һ�����У�ˮ���Ӽ�ľ��벻��ȫ��ȣ�����1��ˮ����������4����ˮ���Ӽ�����ʺ��γ�������γ�����Ļ���ȹ�̬�����٣�C��ȷ��
D�����¶ȴﵽһ����ֵʱ����Һ�����е�ˮ�������²�����ӵ�������ƻ���ʹһ����ˮ�����ܹ������������Ӷ������������Ե�ˮ����������ɱ���们��D��ȷ��
��ѡA��


 ��������������������ϵ�д�
��������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£������������Ϊ 1.0L�ĺ����ܱ������з�����Ӧ��2CH3OH(g) CH3OCH3(g) + H2O(g) ����˵����ȷ���ǣ� ��
���� ��� | �¶�(��) | ��ʼ���ʵ���(mol) | ƽ�����ʵ���(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
II | 387 | 0.40 | ||
III | 207 | 0.20 | 0.090 | 0.090 |
A. �÷�Ӧ������ӦΪ���ȷ�Ӧ
B. �ﵽƽ��ʱ������I�е�CH3OH�������������II�е�С
C. ����I�з�Ӧ����ƽ������ʱ�������III�ij�
D. ����ʼʱ������I�г���0.15mol ��CH3OH��0.15mol ��CH3OCH3��0.10mol ��H2O����Ӧ��������Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾA��F����������
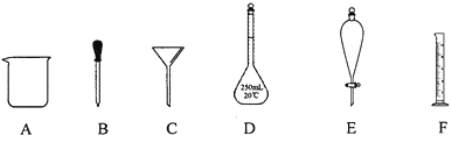
��1��C��___��������������գ���ͬ����D��___�����þƾ��Ƽ��ȵ���___��
��2������ʵ��������õ�����E����___��ѡ������ѡ��ı����ĸ����
a������ˮ��CC14�Ļ���� b������ˮ�;ƾ��Ļ���� c������ˮ����ɰ�Ļ����
��3��ʵ��������һ�����ʵ���Ũ�ȵ����ᣬ�����ܶ�Ϊ1.25g mL-1�� 37%��Ũ����4.5mL��
��ȡ��4.5mL����ʱ����Ҫ�õ����������е�F��___��ѡ�������ı����ĸ����
��ȡ��4.5mL���ᣬ����D��250mL������������һ�����ʵ���Ũ�ȵ����ᣬ��ȷ������õ��������ʵ���Ũ��Ϊ___mol/L������2λ��Ч���֣���
����������У���ʹ������ҺŨ��ƫ�ߵ���___������ţ���
A����ȡ��������۲�Һ��ʱ���� B������ƿ������������ˮ
C��������ˮʱ�����������˿̶��� D������ʱ���ӿ̶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���ѧ�Һϳɵĸ��Ļ����ͨ���������[ph3C]+[B(C6F5)4]-�����ϩ�ۺϱ���ϺõĴ����ԡ��ϳ����Ļ����������һ����Ӧ���£��÷�Ӧ�漰H��C��N��O��Cl��Cr�ȶ���Ԫ�ء�

�ش��������⣺
(1)����״̬�����У����������һ��������������������_____________(����)��
A��![]() B��
B��![]()
C��![]() D��
D��![]()
(2)����������̼ԭ�Ӳ�ȡ���ӻ���ʽΪ______�����������a��b��n��m���Ļ�ѧ������λ������______(����ĸ)����
(3)Cr3+���н�ǿ���ȶ��ԣ�Cr3+�ĺ�������Ų�ʽΪ______����֪û��δ�ɶ�d���ӵĹ��ɽ��������γɵ�ˮ����������ɫ�ģ�Ti4+��V3+��Ni2+�������ӵ�ˮ������Ϊ����ɫ����______(�����ӷ���)��
(4)ClO3-�ļ���С��ClO4-�ļ��ǣ�ԭ����______��
(5)���ݽṹ�����ʵĹ�ϵ���ͣ�HNO2�����Ա�HNO3����ԭ��______��
(6)ˮ�ںϳɸ��Ļ�����Ĺ��������ܼ����о�����ˮ�������13�����͵Ľᾧ�塣�����ر�(�ܶȱ�ˮ��)����������ϵ��������������x��y��z���ͶӰͼ��ͼ��ʾ�������е�H2O��λ��Ϊ_____�����߳�Ϊa pm�����ر����ܶ�Ϊ ____g��cm-3��д����ѧ����ʽ��NAΪ����٤����������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������þ��Mg3N2����һ�ָ�ǿ�ȸ�ұ�������Ӽ�����ijѧϰС����������װ���Ʊ���������þ��
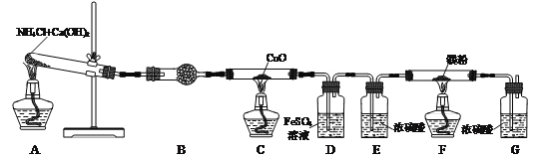
��֪����3Mg��N2![]() Mg3N2����Mg3N2��6H2O=3Mg(OH)2��2NH3��
Mg3N2����Mg3N2��6H2O=3Mg(OH)2��2NH3��
��1������װ�������Եķ�����___��
��2��д��װ��A�з�����Ӧ�Ļ�ѧ����ʽ��___��װ��B���Լ���������___��
��3����Ӧһ��ʱ���װ��C�к�ɫ�����Ϊ��ɫ������ˮ����֡�װ��C�з�����Ӧ�Ļ�ѧ����ʽΪ___��
��4��װ��D��FeSO4��Һ��������___��
��5��ʵ�������װ��A��FӦ���ȼ��ȵ���___����
��6��װ��F���е���þ���ɣ�д��ͨ��ʵ����֤����þ���ɵIJ���������ȡ����װ��F��Ӧ��Ĺ������Թ��У�___��˵�����к�����þ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ����FeSO4��HNO3��������ʵ�飬������Һ������ɫ��������������ɵ�NO2��NO��Fe2+��Fe3+��Ӧ��ʹ��Һ��Ϊ����ɫ���������װ��̽��������˵���������
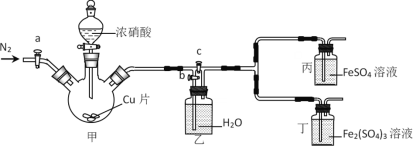
A.�ȼ��װ�������ԣ�����ҩƷ�ر�c����a��b����ͨ��һ��ʱ��N2
B.�ر�a��c����b����Һ©����������Ӧ�������Һ��Ϊ����ɫ��������Һ�����Ա仯��֤��NO��Fe2+��Ӧ
C.���з�Ӧһ��ʱ����±��������Լ����ر�a��b����c����Ӧ�������Һ��Ϊ����ɫ��������Һ�����Ա仯��֤��NO2Ҳ����Fe2+��Ӧ
D.��ʵ���ȱ����ȱ��β������װ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ������˿��Cl2Ϊԭ�Ͻ�����������ʵ�顣���дӷ���Ƕȷ�����ȷ����
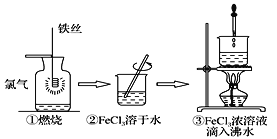
A.ʵ��١��۷�Ӧ�Ƶõ����ʾ�Ϊ������
B.�۷�����ѧ�仯�����յõ��ķ�ɢϵΪ����
C.�ٷ�Ӧ����˿Ϊ��ԭ����������ԭ��Ӧ
D.ʵ��١����漰���������ʾ�Ϊ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̼����[CO(NH2)2H2O2]��һ�ָ�Ч����ȫ�Ĺ�������������ɫ���壬������ˮ���Ը��¶�ʱ�ɷ����ֽ⡣ij��ѧС�����Ʊ�����������̼���������ⶨ��������ĺ������ش��������⡣
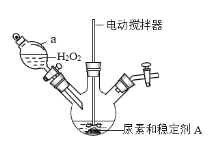
(һ)������̼�������Ʊ�
(1)�Ʊ�������̼�����ķ���װ����ͼ��ʾ(�г�װ����ȥ)������װ����ǰӦ��aװ�ý��еIJ�����________��
(2)�÷�Ӧ������¶�Ϊ35�������õĺ��ʼ��ȷ�ʽΪ________��
(��)������̼�����л����������IJⶨ(�Բ�Ʒ�й�������������ԭ�ӵ���������Ϊ����)����ȡ10.0g��Ʒ�����250mL��Һ��ȡ25.00mL��Һ����ƿ�У���������ϡ���ᣬ��0.10molL��1������ر���Һ�ζ����Σ����ĸ��������Һ������ֱ�Ϊ21.02mL��21.23mL��20.98mL��
(1)д��KMnO4����Һ��H2O2��Ӧ�Ļ�ѧ����ʽ____________��
(2)������̼�����л���������Ϊ_____%�������ƹ�����̼������Һ����ʱ���ӿ̶��ߣ����ù�����̼�����л���������______(����ƫ������ƫ����������Ӱ����)��
(��)�ȶ���A�Թ�����̼�������Ʊ���һ����Ӱ�죬С���Ա�����������ϵõ��й��ȶ��������������ʾ����ѡ������ȶ���AΪ________��������_____________��
�ȶ������� | ������̼�����������ĺ���/10��2 | ||||
��ʼ�� | ���´���30����� | ������ | �ȴ��汣��1����� | ������ | |
EDTA | 16.96 | 16.87 | 0.09 | 16.92 | 0.04 |
������ | 16.94 | 16.90 | 0.04 | 16.91 | 0.03 |
EDTA������������ | 16.95 | 16.90 | 0.05 | 16.90 | 0.05 |
�������뽹�����ƻ���� | 16.90 | 16.86 | 0.04 | 16.87 | 0.03 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º��ݵ������н��з�ӦN2(g)��3H2(g) ![]() 2NH3(g)��������Ũ����0.1 mol��L-1����0.06 mol��L-1��2 s����ô��0.06 mol��L-1����0.024 mol��L-1��Ҫ�ķ�Ӧʱ��Ϊ
2NH3(g)��������Ũ����0.1 mol��L-1����0.06 mol��L-1��2 s����ô��0.06 mol��L-1����0.024 mol��L-1��Ҫ�ķ�Ӧʱ��Ϊ
A. ����1.8 s B. ����1.2 s C. ����1.8 s D. ��1.8 s
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com