
| A. | 在铁件上镀铜时,金属铜作阴极 | |
| B. | 甲醇和氧气以及KOH溶液构成的新型燃料电池中,其负极上发生的反应为CH3OH+6OH-+6e-═CO2+5H2O | |
| C. | 纯锌与稀硫酸反应时,加入少量CuSO4溶液,可使反应速率加快 | |
| D. | 电解精炼铜时,电解质溶液中铜离子浓度保持不变 |
分析 A.电镀时,镀层作阳极、镀件作阴极;
B.甲醇燃料碱性电池中,负极上生成碳酸根离子而不是二氧化碳;
C.原电池能加快负极金属被腐蚀速率;
D.电解精炼粗铜时,电解质溶液中铜离子浓度减小.
解答 解:A.电镀时,镀层作阳极、镀件作阴极,所以在铁件上镀铜时,镀层Cu作阳极、镀件Fe作阴极,故A错误;
B.甲醇燃料碱性电池中,负极上生成碳酸根离子而不是二氧化碳,负极反应式为2CH3OH+3O2+4OH-→2CO32-+6H2O,正极反应为:O2+2H2O+4e-=4OH-,故B错误;
C.原电池能加快负极金属被腐蚀速率,Zn置换出Cu,Zn、Cu和稀硫酸构成原电池且Zn作负极,所以加快Zn被腐蚀速率,故C正确;
D.电解精炼粗铜时,阳极上不仅有铜还有比铜活泼的金属失电子,阴极上只有Cu析出,所以阴极析出的铜质量大于阳极溶解的铜质量,则电解质溶液中铜离子浓度减小,故D错误;
故选C.
点评 本题考查电解原理,为高频考点,明确各个电极上发生的反应及原电池对化学反应速率的影响是解本题关键,注意电解精炼与电镀的区别,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝基苯是一种油状物质,会浮在水面上 | |
| B. | 实验室制硝基苯需要用水浴加热,控制温度在50℃~60℃ | |
| C. | 硝基苯中毒是由蒸气吸入或误食引起的,与皮肤接触不会引起中毒 | |
| D. | 硝基苯是由甲苯和硝酸直接反应生成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ②③④ | C. | ②⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ③⑥ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 第2周期 | ⑤ | ⑦ | ⑨ | |||||
| 第3周期 | ① | ③ | ⑥ | ④ | ⑧ | ⑩ | ||
| 第4周期 | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
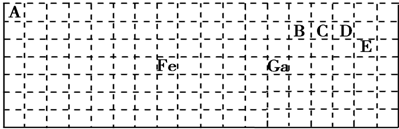
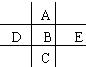 如图为周期表前四周期的一小部分,A、B、C、D、E的位置关系如图所示.其中B元素的最高价是负价绝对值的3倍,它的最高氧化物中含氧60%,回答下列问题:
如图为周期表前四周期的一小部分,A、B、C、D、E的位置关系如图所示.其中B元素的最高价是负价绝对值的3倍,它的最高氧化物中含氧60%,回答下列问题: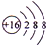 .A单质的电子式为
.A单质的电子式为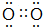 .
.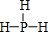 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烷 | B. | 新戊烷 | C. | 正丁烷 | D. | 异丁烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com