
| A、KHCO3 |
| B、K2CO3和Na2CO3 |
| C、MgCO3和Na2CO3 |
| D、Na2CO3和NaHCO3 |
| 12 |
| 100 |
| 12 |
| 100 |
| 12 |
| 100 |
| 12 |
| 100 |
| 12 |
| 100 |
| 12 |
| 100 |
| 12 |
| 106 |
| 12 |
| 84 |
| 12 |
| 106 |
| 12 |
| 84 |


科目:高中化学 来源: 题型:
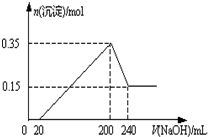 将一定质量的Mg和Al的混合物投入2.0mol/L,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入一定浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示.回答下列问题:
将一定质量的Mg和Al的混合物投入2.0mol/L,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入一定浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为防止富脂食品氧化变质,常在包装袋中放入生石灰 |
| B、“天宫一号”中使用的碳纤维,是一种新型无机非金属材料 |
| C、用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
| D、汽车排放的尾气和冬季取暖排放颗粒污染物是形成雾霾的重要因素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0.20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.24 | 0.24 | 0.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用酚酞溶液鉴别稀盐酸和稀氢氧化钠溶液 |
| B、用燃着的木条鉴别CO2和O2 |
| C、用稀硫酸鉴别锌片和铜片 |
| D、用加水溶解的方法即可鉴别食盐和白糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用淀粉溶液鉴别NaBr、KI溶液 |
| B、用KMnO4酸性溶液鉴别CH4、C2H4气体 |
| C、用AgNO3溶液鉴别Na2SO4、NaCl溶液 |
| D、用澄清石灰水鉴别Na2CO3、NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 100mL盐酸 | 100mL盐酸 | 100mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标准状况) | 2.24L | 3.36L | 3.36L |
| A、盐酸物质的量浓度为1.5mol/L |
| B、15.7g混合物与盐酸反应后有剩余 |
| C、加入9.2 g混合物时消耗HCl 0.1mol |
| D、混合物中NaHCO3和KHCO3的质量比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com