
 (1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.分析 (1)二氧化锰与浓盐酸在加热条件下反应生成氯化锰和氯气、水;
(2)氯气不具有漂白性,具有漂白性的为次氯酸;
(3)氢氧化钙与氯气反应生成氯化钙、次氯酸钙和水;次氯酸钙与二氧化碳和水反应生成次氯酸和碳酸钙;
(4)氧化还原反应中所含元素化合价升高的反应物为还原剂,元素化合价降低的反应物为氧化剂,依据方程式判断.
解答 解:(1)二氧化锰与浓盐酸在加热条件下反应生成氯化锰和氯气、水,离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
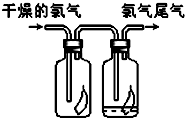
(2)氯气不具有漂白性,具有漂白性的为次氯酸,所以干燥的氯气依次通过盛有干燥的有色布条的广口瓶A和盛有潮湿的有色布条的广口瓶B,可观察到的现象是:A瓶中布条不褪色、B瓶中布条褪色;
故答案为:A瓶中布条不褪色、B瓶中布条褪色;
(3)氢氧化钙与氯气反应生成氯化钙、次氯酸钙和水,化学方程式:Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O;次氯酸钙与二氧化碳和水反应生成次氯酸和碳酸钙,化学方程式:Ca(ClO)2+H2CO3=CaCO3↓+2HClO
故答案为:Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O;Ca(ClO)2+H2CO3=CaCO3↓+2HClO;
(4)3Cl2+8NH3═N2+6NH4Cl,反应中3mol氯气中0价的氯原子化合价都降低,所以氧化剂物质的量为3mol,8氨气中有2mol氨气中的-3价的N化合价升高为0,所以还原剂的物质的量为2mol,所以氧化剂与还原剂的物质的量之比为3:2;
故答案为:3:2.
点评 本题考查了氯气的制备及性质的检验,明确氯气制备原理及性质是解题关键,注意氧化还原反应中氧化剂、还原剂的判断,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | HCO3-一定不能大量存在 | B. | pH一定是12 | ||
| C. | 加入铝片一定能产生氢气 | D. | 一定不是NH4Cl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成,该溶液中一定含有SO42- | |
| B. | 向某溶液中加入烧碱溶液,加热,用湿润红色石蕊试纸检验,石蕊试纸变蓝色,该溶液中一定含有NH4+ | |
| C. | 向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中加入几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+ | |
| D. | 向某溶液中加入硝酸酸化的硝酸银溶液,有白色沉淀生成,该溶液中一定含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3为红棕色粉末,常作红色油漆和涂料 | |
| B. | SiO2能溶于HF和NaOH,所以SiO2是两性氧化物 | |
| C. | 氧化铝是白色难溶于水的固体,可用于制作耐火材料 | |
| D. | NO不溶于水,与氧气可以反应生成红棕色NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯离子的结构示意图: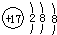 | |
| B. | 作为相对原子质量测定标准的碳核素:${\;}_6^{14}$C | |
| C. | 氯化镁的电子式: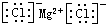 | |
| D. | 乙烯结构简式CH2=CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{4}{100+2.3}$×100% | B. | $\frac{2.3}{100+2.3-1.8}$×100% | ||
| C. | $\frac{2.3}{100+4}×100%$ | D. | $\frac{4}{100+2.3-0.1}$×100% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2CH3 | B. | CH3CH(CH3)2 | C. | C(CH3)4 | D. | CH3CH(CH3)CH2CH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com