
| A. | 硝酸、亚硫酸和次氯酸都是见光易分解的挥发性酸 | |
| B. | 合金属于金属单质,很多性能与组成它的纯金属不同 | |
| C. | 金属及其氧化物、氢氧化物都不可能与强碱溶液反应 | |
| D. | 元素的非金属性、金属性强弱与其得失电子数目无直接关系 |
分析 A.亚硫酸见光不易分解;
B.合金的很多性能与组成它们的纯金属不同;
C.铝能与强碱反应;
D.元素非金属性越强,原子越容易获得电子,元素原子最外层电子数多,元素的非金属性不一定强.
解答 解:A.亚硫酸见光不易分解,硝酸和次氯酸见光易分解,故A错误;
B.合金的很多性能与组成他们的纯金属不同,使合金的用途更加大广泛,合金的性能比组成它的纯金属的性能优良,故B错误;
C.铝、三氧化二铝、氢氧化铝能与强碱反应,故C错误;
D.元素原子最外层电子数多,元素的非金属性不一定强,如I原子最外层电子数为7,O原子最外层电子数为6,非金属性O>I,故D正确.
故选D.
点评 本题侧重考查元素周期律,结构性质位置关系、非金属性比较等,难度不大,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时,立即用水灭火 | |
| B. | 配制稀硫酸时将水倒入浓硫酸中 | |
| C. | 用点燃的火柴在液化气钢瓶口检验是否漏气 | |
| D. | 大量氯气泄漏时,迅速离开现场并尽量往高处走 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
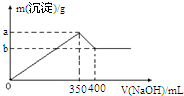 金属及其化合物在化学中扮演着重要的角色,同学们应该熟练掌握它们的性质.
金属及其化合物在化学中扮演着重要的角色,同学们应该熟练掌握它们的性质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含SO2的烟气可用石灰乳吸收后再排放,以减少对空气污染 | |
| B. | 汽车尾气、工业排放、建筑扬尘、垃圾焚烧等都是造成雾霾天气的主要原因 | |
| C. | 绿色化学的核心是对环境产生的污染进行治理 | |
| D. | PM2.5由于颗粒小,在空气中存在时间长,对人体健康危害大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 实验装置图 | 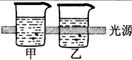 |  | 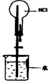 | 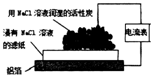 |
| 实验现象 | 乙装置中有亮光通路,甲装置无明显现象 | 关闭止水夹,捂住圆底烧瓶,导管中水柱上升后静止不动 | 打开止水夹,挤压胶头滴管中的水,有喷泉产生 | 电流表指针发生偏转 |
| 实验结论 | 甲装置中分散系不是胶体,乙装置中分散系为胶体 | 该装置气密性良好 | HCl易溶于水 | 电子从铝箔流出,经电流表、活性炭、滤纸回到铝箔 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Cu2+、SO42-、OH- | B. | K+、Ba2+、Cl-、NO3- | ||
| C. | K+、Ca2+、Cl-、MnO4- | D. | Na+、CO32-、SO42-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)3;Fe2O3 | B. | Fe(OH)2;FeO | ||
| C. | Fe(OH)3Fe(OH)2;Fe2O3 | D. | Fe2O3;Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
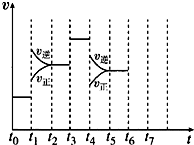 在一密闭容器中发生反应N2+3H2?2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
在一密闭容器中发生反应N2+3H2?2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com