
下列说法中不正确的是 ( )。
A.当两种原子的电负性相差很大时,相互之间通常形成离子键
B.不含金属元素的化合物不一定是共价化合物
C.HCl分子中的共价键是由氢原子的1s轨道和氯原子的3s轨道重叠形成的
D.四氯化碳分子中含四个共价单键,为正四面体
科目:高中化学 来源: 题型:
(1)估计下列各变化过程是熵增还是熵减。
①NH4NO3爆炸:2NH4NO3(s)===2N2(g)+4H2O(g)+O2(g)
②水煤气转化:CO(g)+H2O(g)===CO2(g)+H2(g)
③臭氧的生成:3O2(g)===2O3(g)
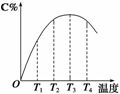
(2)可逆反应A(g)+B(g)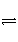
 2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如右图所示。
2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如右图所示。
①由T1向T2变化时,正反应速率______逆反应速率(填“>”、“<”或“=”)。
②由T3向T4变化时,正反应速率______逆反应速率(填“>”、“<”或“=”)。
③反应在________温度下达到平衡。
④此反应的正反应为______热反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、黏合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OH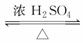 CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有:__________、__________等。
(2)若用如图所示的装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为________、________等。
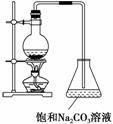
(3)此反应以浓硫酸为催化剂,可能会造成__________、__________等问题。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
| 同一反应时间 | 同一反应温度 | |||||
| 反应温度/℃ | 转化率(%) | 选择性(%)* | 反应时间/h | 转化率(%) | 选择性(%)* | |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 | |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 | |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 | |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
①根据表中数据,下列________(填字母)为该反应的最佳条件。
A.120 ℃,4 h B.80 ℃,2 h
C.60 ℃,4 h D.40 ℃,3 h
②当反应温度达到120 ℃时,反应选择性降低的原因可能为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在固定体积的密闭容器中通入N2和H2,下列能说明达到平衡的是________。
A.3v(N2)=v(H2)
B.断裂1个N≡N的同时断裂6个N—H
C.N2、H2、NH3的物质的量之比是1∶3∶2
D.容器内气体的压强不变
E.气体的密度不变
F.气体的平均相对分子质量不变
(2)在2 L的密闭容器中通入2 mol N2、8 mol H2,5 min时达到平衡,测得NH3的物质的量是2 mol,则平衡时c(H2)=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-===Cl2↑
B.氢氧燃料电池的负极反应式为:O2+2H2O+4e-===4OH-
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-===Cu2+
D.钢铁发生电化学腐蚀的正极反应式为:Fe-2e-===Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,通电5 min后,电极5的质量增加了2.16 g,回答:
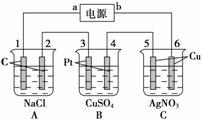
(1)电源:a是________极,C池是________池。
A池阳极电极反应式为__________________,阴极电极反应式为__________________。C池阳极电极反应式__________________,阴极电极反应式为
________________________________________________________________________。
(2)如果B槽中共收集到224 mL气体(标准状况),且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为
________________________________________________________________________。
(3)如果A池溶液也是200 mL(电解过程中溶液体积不变),则通电后,溶液的pH为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
皂化反应实验的操作步骤如下:
(1)在小烧杯中加入约5 g 新鲜的动物脂肪(如牛油)和6 mL 95%的乙醇,微热使脂肪完全溶解;
(2)在(1)的混合液中加入6 mL 40%的氢氧化钠溶液,边搅拌边加热,直至反应液变成黄棕色黏稠状;
(3)用玻璃棒蘸取反应液,滴入装有热水的试管中,振荡,若无油滴浮在液面上,说明反应液中油脂已完全反应,否则要继续加热使之反应完全;
(4)在另一只烧杯中加入60 mL 热的饱和食盐水,把得到的反应液倒入食盐水中,搅拌,观察浮在液面上的固体物质,取出,用滤纸或纱布吸干,挤压成块,并与日常使用的肥皂比较去污能力的大小。
根据上面的实验步骤,请回答下列问题:
(1)加入乙醇的原因是______________________________________________________。
(2)请写出硬脂酸甘油酯发生皂化反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于晶体的自范性,下列叙述正确的是 ( )。
A.破损的晶体能够在固态时自动变成规则的多面体
B.缺角的氯化钠晶体在饱和NaCl溶液中慢慢变为完美的立方体块
C.圆形容器中结出的冰是圆形的体现了晶体的自范性
D.由玻璃制成规则的玻璃球体现了晶体的自范性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com