
| A. | C | B. | NH3 | C. | Mg | D. | S |
分析 A.C与氧气反应生成一氧化碳,一氧化碳与氧气反应生成二氧化碳;
B.NH3与氧气反应生成一氧化氮,一氧化氮氧化生成二氧化氮;
C.Mg与氧气反应生成MgO,MgO与氧气不反应;
D.硫与氧气反应生成二氧化硫,二氧化硫与氧气反应生成三氧化硫.
解答 解:A.C与氧气反应生成一氧化碳,一氧化碳与氧气反应生成二氧化碳,X为C能实现如图所示转化关系,故A不选;
B.NH3与氧气反应生成一氧化氮,一氧化氮氧化生成二氧化氮,X为NH3能实现如图所示转化关系,故B不选;
C.Mg与氧气反应生成MgO,MgO与氧气不反应,X为Mg不能实现如图所示转化关系,故C选;
D.硫与氧气反应生成二氧化硫,二氧化硫与氧气反应生成三氧化硫,X为S能实现如图所示转化关系,故D不选;
故选:C.
点评 本题属于无机推断题,考查了物质间的转化,熟悉相关物质的化学性质是解题关键,注意对相关知识的积累.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:推断题
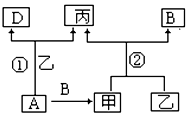 已知A、B、D为单质,其中B、D在常温常压下为气体.甲、乙、丙为常见化合物,甲、丙的焰色反应均为黄色,乙常温下为液体,有关转化关系如图所示:
已知A、B、D为单质,其中B、D在常温常压下为气体.甲、乙、丙为常见化合物,甲、丙的焰色反应均为黄色,乙常温下为液体,有关转化关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
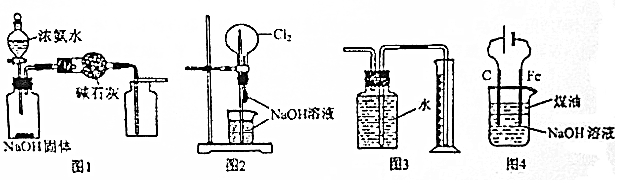
| A. | 图1装置可制取干燥纯净的NH3 | |
| B. | 图2装置可以完成“喷泉”实验 | |
| C. | 图3装置可测量Cu与浓硝酸反应产生气体的体积 | |
| D. | 图4装置可用于实验室制备Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
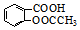 和
和 

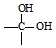 $\stackrel{自动脱水}{→}$
$\stackrel{自动脱水}{→}$
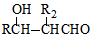 $\stackrel{△}{→}$
$\stackrel{△}{→}$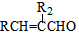 +H2O
+H2O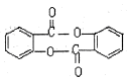 .
.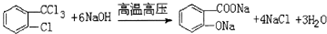 .
.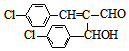 .
.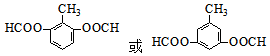 .(任写出一种)
.(任写出一种)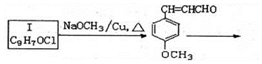
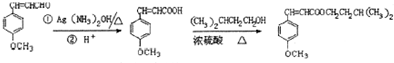 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为防止食品的氧化变质,常在食品包装袋中放入生石灰 | |
| B. | 节日里绚丽的烟花,是通过某些金属元素的化学变化实现的 | |
| C. | SO2具有漂白性,通常用于银耳等食品的漂白 | |
| D. | 干冰或碘化银可用于进行人工降雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该实验过程中要用到氧化剂 | |
| B. | 检验碘单质是否存在,可用碘化钾溶液 | |
| C. | 要萃取碘水中的碘,可以用汽油或酒精 | |
| D. | 利用如图所示装置不能分离食盐和晶体碘的混和物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
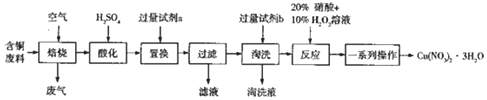
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com