
| A. | 从左到右,金属性减弱 | B. | 从左到右,非金属性增强 | ||
| C. | 从左到右,正化合价的数值增大 | D. | 从左到右,原子半径逐渐增大 |
分析 第三周期元素中,从左到右,随着原子序数的递增,元素金属性减弱、非金属性增强;元素正化合价的数值增大、原子半径逐渐减小,据此进行解答.
解答 解:A.第三周期元素,从左到右,随着原子序数的递增,元素金属性减弱,故A正确;
B.三周期元素,从左到右,随着原子序数的递增,元素非金属性逐渐增强,故B正确;
C.从左到右,正化合价从+1→+7,正化合价的数值增大,故C正确;
D.同一周期中,各元素的电子层数相同,原子序数越大,原子半径越小,故D错误;
故选D.
点评 本题考查元素周期律的作用,题目难度不大,明确元素周期律的内容为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的灵活应用能力.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 化学性质 | 实际应用 |
| A | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
| B | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
| C | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
| D | 乙酸具有酸性 | 常用于去除水垢 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
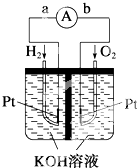 氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法.
氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔的结构式为CH≡CH | B. | 甲烷分子的比例模型为 | ||
| C. | 碳原子的结构示意图为  | D. | 碳原子最外层电子的轨道表示式为 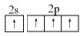 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
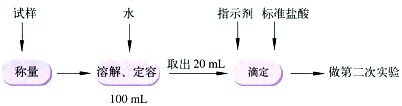
| 物质 | 样品 | 消耗的稀盐酸 | 反应后的溶液 |
| 质量(g) | 4.5g | 37.7g | 40g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯与钠形成离子键,氯与硅形成共价键 | |
| B. | 向淀粉KI溶液中滴加溴水,溶液变蓝 | |
| C. | 向Na2SO3溶液中滴加盐酸,有气泡生成 | |
| D. | F2在暗处遇H2即爆炸,I2在暗处遇H2几乎不反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S2-的结构示意图: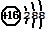 | |
| B. | 过氧化氢的电子式: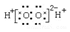 | |
| C. | Ge原子的简化电子排布式:[Ar]4s24p2 | |
| D. | 氯化钠的分子式:NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com