
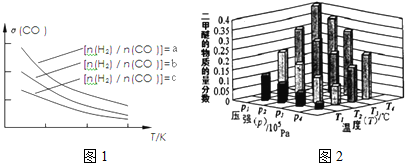
分析 ①增大H2的浓度,平衡右移,CO的转化率增大;
②根据图2温度升高CO的转化率降低分析判断;
根据正反应为气体体积减小的反应,增大压强平衡正向移动,二甲醚的质量分数增大分析判断;
③A.增大反应物浓度,平衡正向移动,正反应速率先增大后减小;
B.逆反应速率先增大后减小,说明平衡逆向移动;
C.化学平衡常数K值增大,说明平衡正向移动;
D.反应物的体积百分含量增大,可以增大反应物浓度市平衡正向移动;
E.移走生成物的量,平衡正向移动,混合气体总质量减小,容器容积不变,混合气体密度减小;
F.增大氢气的物质的量,平衡正向移动,但氢气转化率减小.
解答 解:①增大H2的浓度,平衡右移,CO的转化率增大,故有a>b>c,故答案为:a>b>c;
②通过图2可知,温度升高CO的转化率降低,说明升温平衡逆向移动,故正反应方向为放热反应,则温度越高二甲醚的质量分数越小,故温度:T1>T2>T3>T4;
正反应为气体体积减小的反应,增大压强平衡正向移动,二甲醚的质量分数增大,故压强P1>P2>P3>P4,
故选:BD;
③A.增大反应物浓度,平衡正向移动,正反应速率先增大后减小,不一定逆向移动,故A错误;
B.逆反应速率先增大后减小,说明平衡逆向移动,故B正确;
C.化学平衡常数K值增大,说明平衡正向移动,故C错误;
D.反应物的体积百分含量增大,可以增大反应物浓度市平衡正向移动,故D错误;
E.移走生成物的量,平衡正向移动,混合气体总质量减小,容器容积不变,混合气体密度减小,故E错误;
F.增大氢气的物质的量,平衡正向移动,但氢气转化率减小,故F错误,
故选:B.
点评 本题考查化学平衡图象、平衡状态建立、平衡移动等,对学生综合能力考查,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 1.5 g甲基(-CH3)所含电子数目为NA | |
| B. | 0.1 mol Mg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA | |
| C. | 由2H和18O所组成的水11 g,其中所含的中子数为5NA | |
| D. | 1 mol Fe溶于过量硝酸,电子转移数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率关系是:2υ正(NH3)=3υ正(H2O) | |
| B. | 达到化学平衡时,4υ正(O2)=5υ逆(NO) | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在用蒸馏水洗涤烧杯时,洗液未全部注入容量瓶中 | |
| B. | 用量筒量取浓硫酸时,俯视刻度线 | |
| C. | 用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理 | |
| D. | 定容时俯视刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水、氢氧化钾溶液、稀盐酸 | B. | 水、氢氧化钠溶液、稀盐酸? | ||
| C. | 水、硝酸银溶液、稀硝酸 | D. | 水、氢氧化钾溶液、稀硝酸? |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
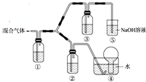 A、B、C、D、E五种短周期元素(A、B、C、D、E分别代表元素符号),它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的$\frac{3}{4}$倍;C与E同主族.
A、B、C、D、E五种短周期元素(A、B、C、D、E分别代表元素符号),它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的$\frac{3}{4}$倍;C与E同主族.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com