
同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
P4(白磷,s)+5O2(g)===P4O10(s) ΔH1=-2 983.2 kJ·mol-1①
P(红磷,s)+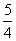 O2(g)===
O2(g)===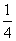 P4O10(s) ΔH2=-738.5 kJ·mol-1②
P4O10(s) ΔH2=-738.5 kJ·mol-1②
则白磷转化为红磷的热化学方程式为____________________________。相同状况下,能量状态较低的是________;白磷的稳定性比红磷________(填“高”或“低”)。
科目:高中化学 来源: 题型:
同温同压下,等体积的两容器内分别充满由14N、13C、18O三种原子构成的一氧化氮和一氧化碳,下列说法正确的是( )
A.所含分子数和质量均不相同
B.含有相同的分子数和电子数
C.含有相同的质子数和中子数
D.含有相同数目的中子、原子和分子
查看答案和解析>>
科目:高中化学 来源: 题型:
用如下图所示装置探究碳酸和苯酚的酸性强弱,下列叙述不正确的是(部分夹持仪器省略)( )
A.②中试剂为饱和NaHCO3溶液
B.打开分液漏斗旋塞,①中产生无色气泡,③中出现白色浑浊
C.苯酚有弱酸性,是由于苯基影响了与其相连的羟基的活性
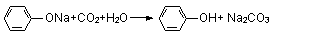 D.③中发生反应的化学方程式是
D.③中发生反应的化学方程式是
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质用途的说法不正确的是
A.明矾可用于自来水的消毒净化
B.Fe2 O3可用作红色油漆和涂料
C.酚醛树脂可用作绝缘、隔热和复合材料
D.硫酸可用于精炼石油以及制取多种挥发性酸
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W为短周期元素且原子序数依次增大。X的一种气态氢化物m可用来焊接或切割金属,且该分子所有原子在一条直线上。Y2-的M能层的原子轨道为全空状态。Z的单质用作铝热反应的引燃剂。 W与X形成的化合物是一种常见的有机溶剂n 。A为第四周期元素,其基态原子含有6个未成对电子。
请回答下列问题:
(1)X在元素周期表中的位置是 。
(2)A3+的外围电子排布式是 。
(3)X、Y、Z形成的晶胞结构示意图如右,则它的化学式是 。
(4)m分子中,X的原子轨道杂化类型是 ,n的分子构型是 。
(5)气体m和含A2Y 的酸性溶液,可通过惰性电极连接构成高能原电池,该电池的正极反应式是 。
的酸性溶液,可通过惰性电极连接构成高能原电池,该电池的正极反应式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
能源问题是人类社会面临的重大课题,H2、CO、CH3OH都是重要的能源物质,它们的燃烧热依次为-285.8 kJ·mol-1、-282.5 kJ·mol-1、-726.7 kJ·mol-1。已知CO和H2在一定条件下可以合成甲醇CO(g)+2H2(g)===CH3OH(l)。则CO与H2反应合成甲醇的热化学方程式为( )
A.CO(g)+2H2(g)===CH3OH(l) ΔH=-127.4 kJ·mol-1
B.CO(g)+2H2(g)===CH3OH(l) ΔH=127.4 kJ·mol-1
C.CO(g)+2H2(g)===CH3OH(g) ΔH=-127.4 kJ·mol-1
D.CO(g)+2H2(g)===CH3OH(g) ΔH=127.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
关于电解NaCl水溶液,下列叙述正确的是( )

A.电解时在阳极得到氯气,在阴极得到金属钠
B.若在阳极附近的溶液中滴入KI溶液,溶液呈棕色
C.若在阴极附近的溶液中滴入酚酞试液,溶液呈无色
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
空气是人类生存所必需的重要资源。为改善空气质量而启动的“蓝天工程”得到了全民的支持。下列措施不利于“蓝天工程”建设的是 ( )。
A.推广使用燃煤脱硫技术,防止SO2污染
B.实施绿化工程、防止扬尘污染
C.研制开发燃料电池汽车,消除机动车尾气污染
D.加大石油、煤炭的开采速度,增加化石燃料的供应量
查看答案和解析>>
科目:高中化学 来源: 题型:
维生素C(又名抗坏血酸,分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,其含量可通过在弱酸性溶液中用已知浓度的I2溶液进行滴定。该反应的化学方程式如下:C6H8O6+I2―→C6H6O6+2HI。现欲测定某样品中维生素C的含量,具体的步骤及测得的数据如下。取10 mL 6 mol·L-1 CH3COOH溶液,加入100 mL蒸馏水,将溶液加热煮沸后冷却。精确称取0.200 0 g样品,溶解于上述冷却的溶液中,加入1 mL淀粉溶液作指示剂,立即用浓度为0.050 00 mol·L-1的I2溶液进行滴定,直至溶液中的蓝色持续不退为止,共消耗21.00 mL I2溶液。
(1)为何加入的CH3COOH溶液要先经煮沸、冷却后才能使用?
(2)计算样品中维生素C的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com