
| A. | Fe3+、Na+、Cl-、S2-(1:2:3:1) | B. | NH4+、Ba2+、OH-、NO3-(1:1:1:2) | ||
| C. | K+、H+、I-、AlO2-(1:1:1:1) | D. | Na+、Al3+、Cl-、OH-(4:1:4:3) |
分析 A.Fe3+、S2-发生氧化还原反应生成FeS、S;
B.NH4+、OH-结合生成弱碱;
C.H+、AlO2-结合生成沉淀;
D.Al3+、OH-以1:3结合生成沉淀.
解答 解:A.Fe3+、S2-发生氧化还原反应生成FeS、S,不能得到澄清溶液,故A不选;
B.NH4+、OH-结合生成弱碱,且NH4+、Ba2+、OH-、NO3-为1:1:1:2时,遵循电荷守恒,为无色、澄清溶液,故B选;
C.H+、AlO2-结合生成沉淀,不能得到澄清溶液,故C不选;
D.Al3+、OH-以1:3结合生成沉淀,不能得到澄清溶液,故D不选;
故选B.
点评 本题考查离子的共存,为高频考点,把握离子之间的反应及电荷守恒为解答本题的关键,侧重分析与应用的考查,注意生成沉淀时不能得到澄清溶液,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Fe2+为还原剂,NO3-被还原 | |
| B. | 消耗l mol氧化剂,转移电子8 mol | |
| C. | 氧化产物与还原产物的物质的量之比为1:8 | |
| D. | 若把该反应设计为原电池,则负极反应式为 Fe2+-e-=Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
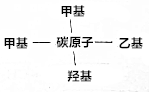 某一元醇的分子式为C5H12O,它的其中一种结构用文字表述为:
某一元醇的分子式为C5H12O,它的其中一种结构用文字表述为:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中还原剂是C,还原产物有两种 | |
| B. | 若有32g硫参加反应,则被硫氧化的碳单质物质的量为3mol | |
| C. | 若在标准状况下生成8.96L气体,则转移的电子数为1.2NA | |
| D. | 产物中的两种气体在一定条件下都能够和Mg发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +
+ $\stackrel{H_{2}SO_{4}}{→}$
$\stackrel{H_{2}SO_{4}}{→}$ ;
;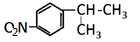 ;A转化为B的反应类型是加成反应.
;A转化为B的反应类型是加成反应.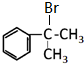 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$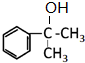 +NaBr.
+NaBr.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2aPa | B. | 2$\sqrt{a}$Pa | C. | $\frac{2}{3}$aPa | D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com