
| A、1molNH3所含有的原子数为NA |
| B、常温常压下,22.4L氧气所含的原子数为2NA |
| C、常温常压下,48gO3所含的氧原子数为3NA |
| D、标准状况下,33.6LH2O含有9.03×1023个H2O分子 |


科目:高中化学 来源: 题型:
| A、将蒸发皿放置在铁架台的铁圈上直接用酒精灯火焰加热 |
| B、将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热 |
| C、用手持着蒸发皿直接用酒精灯火焰加热 |
| D、将灼热的蒸发皿直接用冷水冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18gH2O含有的氢原子数目为NA |
| B、标准状况下,22.4LH2O含有的分子数目为NA |
| C、24g Mg变为Mg2+时失去的电子数为NA |
| D、常温常压下,71gCl2中含有的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5 mol H2O含有的原子数目为1.5 NA |
| B、32 g O2所含的原子数目为NA |
| C、1 mol H2O含有的H2O分子数目为NA |
| D、0.5 NA个氯气分子的物质的量是0.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2(g)+Cl2(g)=2HCl(g)△H=-184.6kJ?mol-1 | ||
| B、CH4(g)+2O2(g)=2H2O(g)+CO2(g)△H=-802.3kJ?mol-1 | ||
C、CO(g)+
| ||
| D、2H2(g)+O2(g)=2H2O(g)△H=-571.6kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
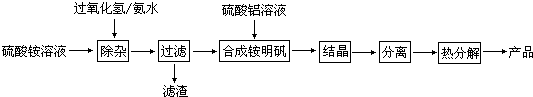
查看答案和解析>>
科目:高中化学 来源: 题型:
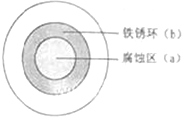
| A、液滴中的Cl-由a 区向b区迁移 |
| B、液滴边缘区发生的电极反应为:2H++2e-=H2 |
| C、液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a 区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D、导致该现象的主要原因是液滴之下氧气含量比边缘处少. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com