
| A. | 分别加水稀释10倍,两溶液的pH仍相等 | |
| B. | 温度升高10℃,两溶液的pH均不变 | |
| C. | 加入适量的氯化铵晶体后,两溶液的pH均减小 | |
| D. | 用相同浓度的盐酸中和至反应完全时,消耗盐酸的体积相同 |
分析 NaOH是强碱,一水合氨是弱碱,室温下,pH相等氨水和NaOH溶液中,氨水浓度大于NaOH,
A、加水稀释促进一水合氨电离;
B、升高温度,一水合氨电离程度增大;
C、加入适量的氯化铵晶体,抑制一水合氨电离,NaOH和氯化铵反应生成氯化钠和一水合氨;
D、用HCl中和,消耗盐酸的体积与碱的物质的量成正比.
解答 解:NaOH是强碱,一水合氨是弱碱,室温下,pH相等氨水和NaOH溶液中,氨水浓度大于NaOH,
A、加水稀释促进一水合氨电离,则稀释后氨水的pH大于氢氧化钠,故A错误;
B、升高温度,一水合氨电离程度增大,所以氨水的pH增大,故B错误;
C、加入适量的氯化铵晶体,抑制一水合氨电离,NaOH和氯化铵反应生成氯化钠和一水合氨,所以加入适量的氯化铵晶体后,两溶液的pH均碱小,故C正确;
D、用HCl中和,消耗盐酸的体积与碱的物质的量成正比,pH相等、体积相等的氨水和氢氧化钠溶液,一水合氨的物质的量大于氢氧化钠,所以氢氧化钠消耗的盐酸少,故D错误;
故选C.
点评 本题考查了弱电解质的电离,明确弱电解质的电离特点是解本题关键,易错选项是D,注意消耗酸的物质的量与碱的物质的量成正比,与电解质强弱无关,为易错点.


 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:解答题

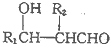 (R1、R2为烃基或H)
(R1、R2为烃基或H)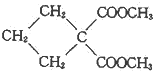 +HBr+HCl
+HBr+HCl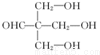 .
. .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
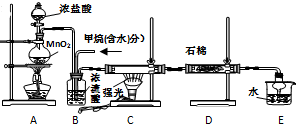
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
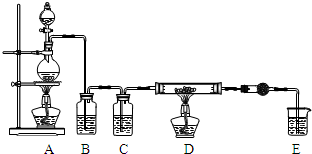
| 第一次实验 | 第二次实验 | 第三次实验 | |
| D中固体用量 | 2.0g | 2.0g | 2.0g |
| 氢气的体积 | 334.5mL | 336.0mL | 337.5mL |
| 步骤 | 实验操作 | 预测现象和结论 |
| ① | 往不再产生氯气的装置中,加入NaCl固体,继续加热 | 若有黄绿色气体生成,则假设1成立 |
| ② | 往不再产生氯气的装置中,加入浓硫酸并继续加热 | 若有黄绿色气体生成,则假设2成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小于$\frac{1}{2}$ | B. | 大于$\frac{1}{2}$,小于1 | C. | 等于$\frac{1}{2}$ | D. | 大于1,小于2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知25℃时部分弱电解质的电离平衡常数数据如下表:
已知25℃时部分弱电解质的电离平衡常数数据如下表:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅的结构式:O=Si=O | |
| B. | H2O沸点高于NH3,是因为H2O分子间存在氢键而NH3分子间不存在氢键 | |
| C. | 含有金属离子的晶体一定是离子晶体 | |
| D. | 分子晶体中一定存在分子间作用力,不一定存在共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com