
【题目】中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
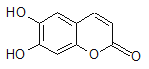
A、2 mol Br2 2 mol NaOH
B、2 mol Br2 3 mol NaOH
C、3 mol Br2 4 mol NaOH
D、4 mol Br2 4 mol NaOH
科目:高中化学 来源: 题型:
【题目】正丁醛经催化加氢可制备1-丁醇。为提纯含少量正丁醛杂质的1-丁醇,现设计如下路线:
![]()
已知:①正丁醛与饱和NaHSO3溶液反应可生成沉淀;②乙醚的沸点是34℃,难溶于水,与1-丁醇互溶;③1-丁醇的沸点是118℃。则操作1~4分别是( )
A.萃取、过滤、蒸馏、蒸馏 B.过滤、分液、蒸馏、萃取
C.过滤、蒸馏、过滤、蒸馏 D.过滤、分液、过滤、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分类或归类正确的是:①铝热剂、纯净矿泉水、冰水混合物均为混合物 ②NaOH、HD、H2O均为化合物③明矾、烧碱、硫酸均为强电解质④C60、金刚石、石墨均为碳的同素异形体⑤碘酒、淀粉溶液、水雾、纳米材料均为胶体
A.①③③⑤ B.③④⑤ C.②④⑤ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。请回答下列问题:
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为 。
(2)W与Y可形成化合物W2Y,该化合物的电子式为 。
(3)Y在周期表中的位置是 。
(4)比较W、X、Y、Z四种元素简单离子的半径大小(用化学式表示,下同): > > > ;比较Y、Z的气态氢化物稳定性强弱: > 。
(5)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为: 。
(6)Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量,写出该反应的热化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国气象局的数据显示,2013年全国平均雾霾天数为52年来之最。形成雾霾的主要成份为:生产生活中排放的废气、汽车尾气及扬尘等。
(1)己知:CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=-4lkJ/mol,某温度下,向容积为2L的密闭容器中充入2.0molCO(g)和2.0mol H2O(g),在tmin时达到平衡,测得放出了32.8kJ热量,则tmin内用H2表示的平均反应速率为_________,由此可知在该温度下反应CO(g)+H2O(g)
CO2(g)+H2(g)△H=-4lkJ/mol,某温度下,向容积为2L的密闭容器中充入2.0molCO(g)和2.0mol H2O(g),在tmin时达到平衡,测得放出了32.8kJ热量,则tmin内用H2表示的平均反应速率为_________,由此可知在该温度下反应CO(g)+H2O(g)![]() CO2(g)+H2(g)的化学平衡常数为_________(保留小数点后一位)。
CO2(g)+H2(g)的化学平衡常数为_________(保留小数点后一位)。
(2)碱式硫酸铝法烟气脱硫工艺主要有以下三步
①向Al2(SO4)3溶液中投入粉末状石灰石,生成碱式硫酸铝[Al2(SO4)3Al2O3]溶液.
②碱式硫酸铝吸收SO2,Al2(SO4)3Al2O3+3SO2=Al2(SO4)3Al2(SO3)3,请写出Al2(SO4)3Al2O3与过量烧碱溶液反应的化学方程式:_________;
③将Al2(SO4)3Al2 (SO3)3氧化成Al2(SO4)3,可选用氧化剂为_________(填代号).
a.浓硫酸 b.KMnO4溶液 C.5%的H2O2溶液 d.空气
该步反应的目的是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要化工原料,其产量是一个国家石油化工水平的标志。请回答:
(一)乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
【工艺甲】![]()
【工艺乙】![]()
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应。因此,上述生产工艺中,应采用工艺__________(填“甲”或“乙”)更环保、更经济。
(二)某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应)。请回答下列问题:
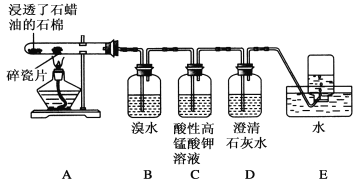
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34![]() C8H18+甲,甲
C8H18+甲,甲![]() 4乙,则甲的分子式为________,乙的结构简式为____________________________________。
4乙,则甲的分子式为________,乙的结构简式为____________________________________。
(2)B装置中的实验现象可能是________,写出反应的化学方程式:________________________,其反应类型是________。
(3)C装置中可观察到的现象是____________,反应类型是________。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置________(填字母)中的实验现象可判断该资料是否真实。为了探究溴与乙烯反应是加成反应而不是取代反应,可以测定装置B中溶液在反应前后的酸碱性,简述其理由: __________________。
(5)通过上述实验探究,检验甲烷和乙烯的方法是________(选填字母,下同);除去甲烷中乙烯的方法是________。
A.气体通入水中
B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶
D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,甲烷火焰明亮而乙烯产生少量黑烟,原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H1N1病毒是一种没有超常抵抗力的病毒.研究证明,许多常用消毒药物如漂粉精、漂白粉、高锰酸钾等,可以将H1N1病毒杀灭.
(1)工业上制取漂白粉的反应方程式为 。
(2)将漂白粉溶于适量水中,呈白色浊状物,静置沉降.取少许上层清液,滴加碳酸钠溶液出现白色沉淀,写出其中一个化学方程式 。另取少许上层清液,滴加适量的 (填化学式)即可检验Cl﹣的存在,发生反应的化学方程式为 。
(3)漂白粉在空气中长期放置,会失效,用化学方程式解释其原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:
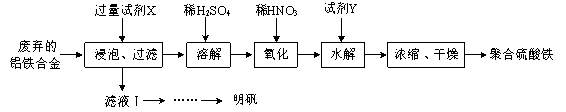
(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH)x(SO4)y]n 中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。
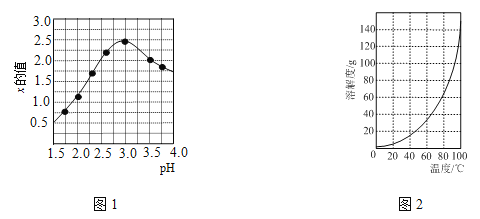
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料, 试剂X应为 。
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生,过滤, 。将溶液 、 、过滤、并用酒精洗涤、干燥,最终得到明矾晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物反应如下图,据此回答下列问题:

(1)乙烯的结构式为: 。
(2)写出反应②④的化学方程式:
② ,反应类型: (1分);
④ ,反应类型: (1分)。
(3)实验室常用下列装置制取乙酸乙酯,请回答相关问题:

①饱和碳酸钠溶液的主要作用是 。
②若要把制得的乙酸乙酯分离出来,应采用的操作是 。
③进行该实验时,最好向试管甲中加入几块碎瓷片,其目的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com