
下列叙述中正确的是
[ ]
A.两个非金属原子间不可能形成离子键
B.非金属原子间只能形成极性共价键
C.离子化合物中可能含有极性共价键也可能含有非极性共价键
D.共价化合物中可能含有离子键
|
解析:两个非金属原子之间绝对不可能得失电子,故不可能形成离子键;而非金属原子组成原子团时,可以形成离子化合物,如铵盐等;在离子化合物中,只要存在原子团,必含有共价键,如 NaOH中的O—H键,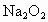 中的O—O键等。而化合物中只要含有离子键就一定是离子化合物。 中的O—O键等。而化合物中只要含有离子键就一定是离子化合物。 |
|
点拨:此类问题的解答,关键在于掌握概念。“两个非金属原子间”与“非金属原子间”有着本质的区别,关系到能否构成原子团。两个 (不同元素)非金属原子只能通过共价键结合,却不能发生得失电子形成离子键。关于离子键与共价键、离子化合物与共价化合物之间的关系,必须明确的是:含有原子团的离子化合物,尽管构成原子团的是共价键,但只要是通过离子键形成的化合物,就一定是离子化合物。 |


科目:高中化学 来源: 题型:
(2013?奉贤区二模)由A、B、C、D四种金属按表中装置进行实验,下列叙述中正确的是( )
| |||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
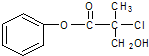 有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )| A、有机物A可以在一定条件下与HBr发生反应 | B、1mol A最多能与4mol H2发生加成反应 | C、有机物A与浓硫酸混合加热,可以发生消去反应 | D、1mol A与足量的NaOH溶液反应,最多可以消耗3mol NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com