
【题目】t℃时,将0.5mol/L的氨水逐滴加入10.00mL0.5mol/L盐酸中,溶液中温度变化曲线Ⅰ、pH变化曲线Ⅱ与加入氨水的体积的关系如图所示(忽略混合时溶液体积的变化)。下列说法正确的是( )

A.Kw的比较:a点比b点大
B.b点氨水与盐酸恰好完全反应,且溶液中c(NH4+)=c(Cl-)
C.c点时溶液中c(NH4+)=c(Cl-)=c(OH-)=c(H+)
D.d点时溶液中c(NH3H2O)+2c(OH-)=c(NH4+)+2c(H+)
【答案】D
【解析】
A.在溶液中存在水的电离平衡,水的电离过程吸收热量,升高温度,水的电离程度增大,Kw增大,根据图示可知,溶液温度b>a,所以Kw:b>a,A错误;
B.HCl与氨水混合,当氨水的体积为10mL时,二者恰好反应产生NH4Cl,该盐是强酸弱碱盐,在溶液中NH4+发生水解反应而消耗,所以溶液中c(NH4+)<c(Cl-),B错误;
C.在c点溶液中存在NH4Cl、H2O,存在电荷守恒,c(NH4+)+c(H+)=c(Cl-)+c(OH-),由于盐电离产生的离子浓度远大于水电离产生的离子浓度,所以溶液中四种离子的浓度不可能相等,C错误;
D.d点时溶液为NH4Cl与氨水等物质的量浓度混合溶液,存在电荷守恒:c(NH4+)+c(H+)=c(Cl-)+c(OH-),同时存在物料守恒:c(NH4+)+c(NH3H2O)=2c(Cl-),将第一个式子扩大2倍,与第二个式子相减,整理可得:c(NH3H2O)+2c(OH-)=c(NH4+)+2c(H+),D正确;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】某实验小组为确定过氧化氢分解的最佳催化条件,用如图实验装置进行实验,反应物用量和反应停止的时间数据如下:
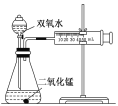
分析表中数据回答下列问题:
MnO2 时间 H2O2 | 0.1g | 0.3g | 0.8g |
10mL1.5% | 223s | 67s | 56s |
10mL3.0% | 308s | 109s | 98s |
10mL4.5% | 395s | 149s | 116s |
(1)相同浓度的过氧化氢的分解速率随着二氧化锰用量的增加而________。
(2)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入________g的二氧化锰为较佳选择。
(3)该小组的某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确________,理由是__________________________________。
(4)为加快过氧化氢的分解速率,除了使用MnO2作催化剂和改变过氧化氢的质量分数之外,还可以采取的加快反应速率的措施有_____。(回答任意两个合理的措施)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将3molA气体和1molB气体通入一密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)请填写下列空白:
xC(g)请填写下列空白:
(1)若容器体积固定为2L,反应2min时测得剩余0.6molB,C的浓度为0.4mol/L。
①2min内,A的平均反应速率为________;x=_______;
②若反应经4min达到平衡,平衡时C的浓度__________0.8mol/L填“大于”、“等于”或“小于”![]() ;
;
(2)若维持容器压强不变:达到平衡时C的体积分数________22%填“大于”、“等于”或“小于”![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列物质中是同系物的有_______;互为同分异构体的有_______________;互为同素异形体的有________________;互为同位素的有_______________;
互为同一物质的有______________;
(1)液氯 (2)氯气 (3)白磷 (4)红磷 (5)D (6)T (7) ![]() (8)
(8)![]() (9)CH2 = CH-CH3 (10)
(9)CH2 = CH-CH3 (10) ![]() (11)2,2—二甲基丁烷
(11)2,2—二甲基丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于在一定条件下进行的化学反应:2SO2+O2![]() 2SO3,改变下列条件,可以提高反应物中活化分子百分数的是 ( )
2SO3,改变下列条件,可以提高反应物中活化分子百分数的是 ( )
A.增大压强B.升高温度C.加入SO2D.减小反应物浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠、铝、铁是三种重要的金属。请回答:
(1)钠元素的金属性比铝的________(填“强”或“弱”)。
(2)将一小块金属钠投入水中,发生反应的离子方程式为______________________;
(3)填写a、b、c化学式并书写①的离子方程式(a、b、c均为含Al化合物);
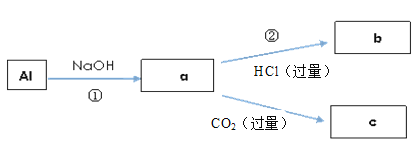
a:__________,b:___________,c:__________;①________;
(4)取一定量的FeCl3,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成________色。
b.向另一支试管中滴加NaOH溶液,反应的离子方程式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色”和“生态文明”是未来的发展主题,而CO2的有效利用可以缓解温室效应,解决能源短缺问题。
(1)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) △H
2CO(g)+2H2(g) △H
已知:反应1 CH4(g)═C(s)+2H2(g) △H1= +75kJ/mol
反应2 2CO(g)═C(s)+CO2(g) △H2=-172kJ/mol
则该催化重整反应的△H=___kJmol-1。
(2)有科学家提出可利用FeO吸收CO2:6FeO(s)+CO2(g)![]() 2Fe3O4(s)+C(s),对该反应的描述正确的是__。
2Fe3O4(s)+C(s),对该反应的描述正确的是__。
A.增大FeO的投入量,利于平衡正向移动
B.压缩容器体积,可增大CO2的转化率,c(CO2)减小
C.恒温恒容下,气体的密度不变可作为平衡的标志
D.恒温恒压下,气体摩尔质量不变可作为平衡的标志
E.若该反应的△H﹤0,则达到化学平衡后升高温度,CO2的物质的量会增加
(3)为研究CO2与CO之间的转化,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g)![]() 2CO(g) H,测得压强、温度对CO的体积分数[φ(CO)%]的影响如图所示,回答下列问题:
2CO(g) H,测得压强、温度对CO的体积分数[φ(CO)%]的影响如图所示,回答下列问题:
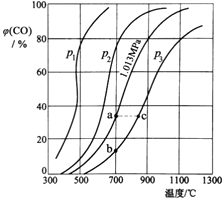
①图中p1、p2、p3的大小关系是______,图中a、b、c三点对应的平衡常数Ka、Kb、Kc的大小关系是______。
②900℃、1.013MPa时,1molCO2与足量碳反应达平衡后容器的体积为VL,CO2的转化率为___(保留一位小数),该反应的平衡常数K=___。
③将②中平衡体系温度降至640℃,压强降至0.1013MPa,重新达到平衡后CO2的体积分数为50%。条件改变时,正反应速率______逆反应速率(填“>”、“<”或“=”)。
(4)在NaOH溶液中通入一定量的CO2气体,所得溶液中c(HCO3-):c(CO32-)=4:1,此时溶液pH=______。(已知:室温下,H2CO3的k1=4×10-7,k2=5×10-11。lg2=0.3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、![]() 、Mg2+、Al3+、Fe3+、
、Mg2+、Al3+、Fe3+、![]() 、
、![]() 、
、![]() 中的几种。
中的几种。
①若加入锌粒,用排空气法收集到无色无味气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法不正确的是( )
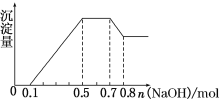
A.溶液中的阳离子有H+、Mg2+、Al3+、![]()
B.溶液中n(Mg2+)=0.1 mol
C.溶液中一定不含![]() 、
、![]() 、Fe3+
、Fe3+
D.n(![]() ∶n(Al3+)∶n(Mg2+)=4∶2∶1
∶n(Al3+)∶n(Mg2+)=4∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。请回答:
(1)基态铜原子的电子排布式为_______________;已知高温下CuO→Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是_________________________。
(2)硒、硅均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,分子构型分别为____________,若“Si—H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se____Si(填“>”、“<”)。
(3)SeO2常温下白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体的晶体类型为_________;若SeO2类似于SO2是V型分子,则Se原子外层轨道的杂化类型为_________。
(4)与镓元素处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3。BF3·NH3中B原子的杂化轨道类型为______,B与N之间形成_________键。
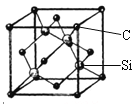
(5)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示;则金刚砂晶体类型为________,在SiC中,每个C原子周围最近的C原子数目为___个;若晶胞的边长为a pm,则金刚砂的密度表达式为_________g/cm3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com