


分析 (1)根据能量变化图,则反应断键共吸收2×630+2×436=2132kJ,形成共放出945+4×463=2797kJ,所以该反应共放出2797-2132=665kJ的热量,据此书写;
(2)①依据化学方程式和平衡常数概念书写平衡常数表达式;
②增加甲醇产率需要平衡正向进行,依据平衡移动原理结合反应特征是气体体积减小的放热反应分析选项判断;
(3)①分析图象的曲线变化特征判断,升高温度,发现NO的分解率降低,说明反应向逆反应方向进行,该反应放热;
②C2H6与NO2发生反应生成无毒的N2、CO2和H2O,由此书写化学方程式;
(4)燃料电池的负极上发生燃料失去电子的氧化反应,即NO2+NO3--e-=N2O5.
解答 解:(1)根据能量变化图,则反应断键共吸收2×630+2×436=2132kJ,形成共放出945+4×463=2797kJ,所以该反应共放出2797-2132=665kJ的热量,热化学方程式为:2NO(g)+2H2(g)=N2(g)+2H2O(g)△H=-665kJ•moL-1,所以氮气和水蒸气反应生成氢气和一氧化氮的热化学方程式是N2(g)+2H2O(g)═2NO(g)+2H2(g)△H=+665 kJ•mol-1,故答案为:N2(g)+2H2O(g)═2NO(g)+2H2(g)△H=+665 kJ•mol-1;
(2)①CO(g)+2H2(g)?CH3OH(g)△H<0,反应的平衡常数为:K=$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$,
故答案为:K=$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$;
②A.升高温度,平衡逆向进行,甲醇产率减小,故A错误;
B.将CH3OH(g)从体系中分离,平衡正向进行,甲醇产率增大,故B正确;
C.充入He,使体系总压强增大,分压不变,平衡不动,故C错误;
故答案为:B;
(3)①升高温度,发现NO的分解率降低,说明反应向逆反应方向进行,该反应放热;由图可知,在$\frac{n(NO)}{n(CO)}$=1的条件下,870℃时,NO还原为N2的转化率为100%,
故答案为:NO分解反应是放热反应,升高温度不利于反应进行;870℃或相近温度;
②C2H6与NO2发生反应生成无毒的N2、CO2和H2O,所以化学方程式为4C2H6+14NO2$\frac{\underline{\;催化剂\;}}{\;}$8CO2+7N2+12H2O,故答案为:4C2H6+14NO2$\frac{\underline{\;催化剂\;}}{\;}$8CO2+7N2+12H2O;
(4)燃料电池的负极上发生燃料失去电子的氧化反应,即NO2+NO3--e-=N2O5,故答案为:NO2+NO3--e-=N2O5.
点评 本题考查了原电池原理、方程式的书写、化学平衡常数、平衡移动等,题目涉及的知识点较多,侧重于考查学生对基础知识的综合应用能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| 选项 | X | Y |
| A | Al | NaOH溶液 |
| B | NO2 | H2O |
| C | Na2O2 | CO2 |
| D | Cu | 浓HNO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 麦芽糖及其水解产物均能发生眼镜反应 | |
| B. | 可用新制Cu(OH)2,鉴别甲酸、乙醛和乙酸 | |
| C. | 用甘氨酸和丙氨酸缩合最多可形成4种二肽 | |
| D. | 淀粉和纤维素互为同分异构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x<y | B. | x=y | C. | x>y | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
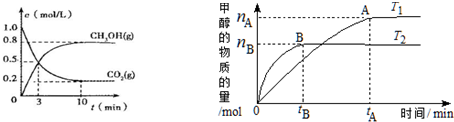
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
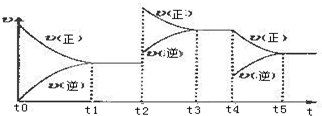
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
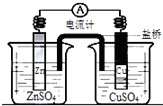
| A. | 铜是阳极,铜片上有气泡产生 | |
| B. | 锌离子在锌片表面被还原 | |
| C. | 正极附近的SO${\;}_{4}^{2-}$离子浓度逐渐增大 | |
| D. | 盐桥中的阳离子会移向CuSO4溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com