
| A. | 元素的简单气态氢化物的热稳定性X<W | |
| B. | 元素的最高价氧化物对应水化物的酸性:W<Z | |
| C. | 化合物YX、ZX2、WX3中化学键类型相同 | |
| D. | 原子半径的大小顺序:Y>Z>W>X |
分析 短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,X有2个电子层,最外层电子数为6,故X为O元素,W与X属于同一主族,故W为S元素,Y原子的最外层只有2个电子,原子序数大于O元素,故Y处于第三周期,故Y为Mg元素,Z单质可制成半导体材料,Z为Si元素,以此解答该题.
解答 解:由以上分析可知X为O、Y为Mg、Z为Si、W为S,
A.非金属性O>S,故元素O的简单气态氢化物的稳定性比S的强,故A错误;
B.非金属Si<S,故元素S的最高价氧化物对应水化物的酸性比Si的强,故B错误;
C.化合物MgO为离子化合物,含有离子键,SiO2、SO3属于共价化合物,含有共价键,故C错误;
D.同周期自左而右,原子半径减小,同主族电子层越多原子半径越大,故原子半径Mg>Si>S>O,即Y>Z>W>X,故D正确,
故选D.
点评 本题考查结构性质与位置关系、元素周期律等,为高考常见题型,侧重考查学生的分析能力,难度不大,推断元素是解题的关键,注意对基础知识的全面掌握.


科目:高中化学 来源: 题型:选择题
| A. | 含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol•L-1 | |
| B. | 常温常压下,5.6g乙烯与丁烯(C4H8)的混合物中氢原子数为0.8NA | |
| C. | 标准状况下,4.48 LCl2与足量的Fe反应转移电子数为0.4NA | |
| D. | 0.1 mol H218O与D2O的混合物中中子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加催化剂同时升高温度 | B. | 加催化剂同时增大压强 | ||
| C. | 升高温度同时充入N2 | D. | 增大压强同时充入NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
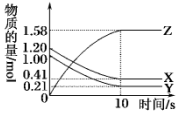 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应开始到10 s,用X表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应开始到10 s,Y的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应10s时达到化学平衡状态,Z的平衡浓度为0.79 mol•L-1 | |
| D. | 反应的化学方程式为2X(g)+2Y(g)?Z(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的二氧化硅可用于制造计算机芯片和太阳能电池 | |
| B. | 胶体和溶液可以通过滤纸进行分离 | |
| C. | 雾是气溶胶,在阳光下可观察到丁达尔效应 | |
| D. | 玻璃是氧化物,成分可表示为Na2O•CaO•6SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=7的溶液中:Al3+、K+、SO42-、HCO3- | |
| B. | FeCl2溶液中:SO42-、H+、MnO4-、Na+ | |
| C. | 水电离的c (H+)=1×10-13 mol•L-1:S2-、SO32-、S2O32-、SO42- | |
| D. | 滴加甲基橙试剂显红色的溶液中:Na+、NH4+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HNO2不跟NaCl反应 | |
| B. | NaNO2溶液的pH大于7 | |
| C. | 常温下0.lmol/L HNO2溶液的pH为2.145 | |
| D. | 相同温度下,用相同浓度的HCl溶液和HNO2溶液作导电试验,HNO2溶液灯泡较暗 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
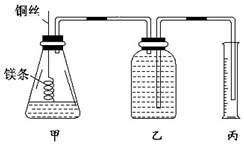 某研究性学习小组欲测定室温下(25℃、101 kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:
某研究性学习小组欲测定室温下(25℃、101 kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com