
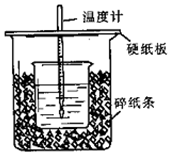
 50 mL 0.50 mol•L-1������50 mL 0.55 mol•L-1NaOH��Һ��ͼʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺
50 mL 0.50 mol•L-1������50 mL 0.55 mol•L-1NaOH��Һ��ͼʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺���� ��1���������ȼƵĹ������жϸ�װ�õ�ȱ��������
��2���к��Ȳⶨʵ��ɰܵĹؼ��DZ��¹�����
��3�����ձ����粻��Ӳֽ�壬��ʹһ��������ɢʧ��
��4����Ӧ�ų����������������Լ�������Ķ����йأ��������к��ȵĸ����ʵ�����ش�
��5������������ʵ������ȷ�����
��6����������кͷ�Ӧ����1molҺ̬ˮʱ�ų�57.3kJ��������д�Ȼ�ѧ����ʽ��
��� �⣺��1�������ȼƵĹ����֪��װ�õ�ȱ�������ǻ��β����������
�ʴ�Ϊ�����β����������
��2���к��Ȳⶨʵ��ɰܵĹؼ��DZ��¹�������С�ձ�֮��������ֽ���������Ǽ���ʵ������е�������ʧ��
�ʴ�Ϊ������ʵ������е�������ʧ��
��3�����ձ����粻��Ӳֽ�壬��ʹһ��������ɢʧ����õ��к�����ֵ�����С��
�ʴ�Ϊ��ƫС��
��4����Ӧ�ų����������������Լ�������Ķ����йأ�����60 mL 0.50 mol•L-1�����50 mL 0.55 mol•L-1NaOH��Һ���з�Ӧ��������ʵ����ȣ�����ˮ�������࣬���ų�������ƫ�ߣ������к��ȵľ���ǿ���ǿ�Ӧ����1molˮʱ�ų����ȣ������������أ����Ը���60 mL 0.50 mol•L-1�����50 mL 0.55 mol•L-1NaOH��Һ����ʵ�飬����к�����ֵ��ȣ�
�ʴ�Ϊ��ƫ����ȣ�
��5��һˮ�ϰ�Ϊ����������Ϊ���ȹ��̣���������ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��Ӧ����Ӧ�ų�������ƫС��
�ʴ�Ϊ��ƫС��
��6��ϡǿ�ᡢϡǿ�Ӧ����1molˮʱ�ų�57.3kJ����������NaOH��Һ�����ᷴӦ��ʾ�к��ȵ��Ȼ�ѧ����ʽΪ��NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H=-57.3 kJ•mol-1��
�ʴ�Ϊ��NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H=-57.3 kJ•mol-1��
���� ���⿼�����к��ȵIJⶨ��������Ŀ�Ѷ��еȣ���ȷ�к��ȵIJⶨ����Ϊ���ؼ���ע�������к��ȼ��㷽��������������ѧ���ķ�����������ѧʵ��������


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �������ù����ռ���Һ����ij�����Al2O3��MgO�������˺�õ���Һ��NaHCO3��Һ�����������ҺpH��Al��OH��3���ɵ��������NaHCO3��Һ����仯���������£������й�˵������ȷ���ǣ�������
�������ù����ռ���Һ����ij�����Al2O3��MgO�������˺�õ���Һ��NaHCO3��Һ�����������ҺpH��Al��OH��3���ɵ��������NaHCO3��Һ����仯���������£������й�˵������ȷ���ǣ�������| A�� | NaHCO3��Һ�����ʵ���Ũ��Ϊ0.8 mol/L | |
| B�� | b����c����Һ������������ͬ | |
| C�� | a����Һ�д��ڵ�������Na+��AlO2-��OH-��H+ | |
| D�� | ���ɳ��������ӷ���ʽΪ��HCO3-+AlO2-+H2O�TAl��OH��3��+CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| HClO | HSCN | H2CO3 |
| K=3.2��10-8 | K=0.13 | K1=4.3��10-7 K2=5.6��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �úϽ���ͭ��þ�����ʵ���֮����2��1 | |
| B�� | ��Ũ������HNO3�����ʵ���Ũ����14.0 mol•L-1 | |
| C�� | �õ�2.54g����ʱ������NaOH��Һ�������600L | |
| D�� | NO2��N2O4�Ļ�������У�NO2�����������80% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ں���������ʵ���Һ�У������ж����ѧƽ��森
�ں���������ʵ���Һ�У������ж����ѧƽ��森�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | �л��� | ͬ���칹����Ŀ |
| A | ����ʽΪC6H14�Һ��������� | 2 |
| B | ����ʽΪC5H10������ʹ������Ȼ�̼��Һ��ɫ | 5 |
| C | ����ʽΪC4H10O��������Na��Ӧ�������� | 4 |
| D | ����ʽΪC4H8O2����NaHCO3��Ӧ�������� | 2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���������㷺����ҩ�Ⱦ�ϡ����ϵȹ�ҵ����ѧ��ѧʵ�鳣��װ�����Ʊ���
���������㷺����ҩ�Ⱦ�ϡ����ϵȹ�ҵ����ѧ��ѧʵ�鳣��װ�����Ʊ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 +HCl
+HCl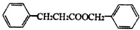 ������M�й����ŵ��Լ���������Һ�����Ʊ�������ͭ��Һ��
������M�й����ŵ��Լ���������Һ�����Ʊ�������ͭ��Һ��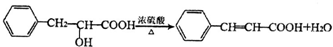 ��
�� ��
��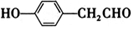 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
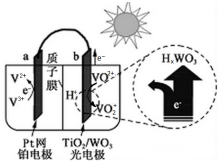
| A�� | ����ʱ��̫������Ҫת��Ϊ���� | |
| B�� | ����ʱ��b���ĵ缫��ӦʽΪVO2+-e-+H2O�TVO2++2H+ | |
| C�� | ����ʱ��ÿת��5 mol���ӣ���5mol H+��b������a����Ǩ�� | |
| D�� | ҹ�䣬a���ĵ缫��ӦʽΪV3++e-�TV2+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com