
【题目】下列说法正确的是( )
A.淀粉、油脂、蛋白质都能发生水解反应
B.蔗糖溶液中加入新制Cu(OH)2煮沸会析出砖红色沉淀
C.纤维素、淀粉都可用(C6H10O5)n表示,它们互为同分异构体
D.人体各种组织的蛋白质不断分解,最终生成二氧化碳和水,排出体外
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若X 最高正价与负价代数和为O,下列说法中不正确的是
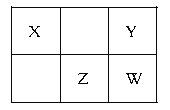
A. 元素X 形成化合物种类最多
B. 元素Y 可形成两种互为同素异形体的单质
C. 元素Z 最高价氧化物可干燥H2、O2等气体
D. 元素宰最高化合价为+7,且其单质具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁分别是氢氧化钙溶液、硝酸钾溶液、碳酸钠溶液、盐酸中的一种.已知甲和丙可以反应,甲和丁也可以反应,则下列说法正确的是( )
A. 甲一定是氢氧化钙溶液 B. 丁只能是盐酸
C. 丙不可能是碳酸钠溶液 D. 乙一定是硝酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)请回答下列问题:
(1)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497 kJ·mol-1.N2(g)+O2(g)=2NO(g)△H=+180.0kJ·mol-1。则相同条件下破坏化学键需要吸收的能量为_______kJ。
(2)25℃时,pH=5的CH3COOH溶液中.由水电离出的氢离子浓度c(H+)=________ kJ·mol-1;往溶液中加入少量NaOH固体,则溶液中![]() _______(填“增大”、“减小”或“不变”),写出表示该混合溶液中所有离子浓度之间的一个等式:_______。
_______(填“增大”、“减小”或“不变”),写出表示该混合溶液中所有离子浓度之间的一个等式:_______。
(3)25℃下,向某Na2CO3溶液中加入稀盐酸,其中含碳元素的各种微粒物质的量分数(φ)随溶液pH变化的部分情况如图所示。
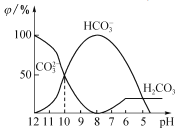
①在同一溶液中,H2CO3、HCO3-、CO32-______(填“能”或“不能”)大量共存。
②当pH =7时,溶液中含碳元素的微粒主要为________。溶液中各种离子的物质的量浓度大小关系为______________。
③反应的CO32-+H2O![]() HCO3-+OH-的平衡常数Kh=______________________。
HCO3-+OH-的平衡常数Kh=______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列应用和相应的原理(用化学方程式表示)及基本反应类型不正确的是( )
A.酒精做燃料:C2H5OH+3O2![]() 2CO2+3H2O 氧化反应
2CO2+3H2O 氧化反应
B.电解水制取氢气:2H2O![]() 2H2↑+O2↑ 分解反应
2H2↑+O2↑ 分解反应
C.敞口放置的氢氧化钠固体变质:2NaOH+CO2=Na2CO3+H2O 复分解反应
D.比较铜和银的活动性:Cu+2AgNO3=Cu(NO3)2+2Ag 置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对牙膏的探究要用到许多化学知识。
(1)下表列出了两种牙膏中的摩擦剂,请在表中填写两种摩擦剂所属的物质类别:
牙膏 | 珍珠王防臭牙膏 | 中华透明牙膏 |
摩擦剂 | 碳酸钙 | 二氧化硅 |
摩擦剂的物质类别(指酸、碱、盐、氧化物) |
(2)根据你的推测,牙膏摩擦剂的溶解性是__________(填“易溶”或“难溶”)。
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。甲同学设计了一种实验室制备碳酸钙的实验方案,其流程如下图所示:
![]()
请写出上述方案中有关反应的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。
(4)乙同学的实验方案为:
![]()
其优点为____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分某化学兴趣小组在实脸室模拟侯德榜制碱法制备纯碱。主要步骤如下:
第一步:配制饱和NaCl溶液,倒入烧杯中加热;
第一步:控制温度在30-35 ℃。边搅拌边分批加入研细的NH4HCO3固体,加料完毕后,继续保温30分钟;
第三步:静置、过滤得NaHCO3晶体.用少量蒸馏水洗涤除去杂质,然后抽干;
第四步:将第二步所得固体转入蒸发皿中,灼烧2小时,制得纯碱固体,
已知:温度高于35℃时,NH4HCO3会分解。有关盐的溶解度(g/100g水)如下表:
盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | —— | —— | —— | —— |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.l | 12.7 | 14.5 | 16.4 | —— |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
回答下列问题:
(1)反应温度控制在30-35℃范围内,应采取的加热方法为 ,反应温度不能高于35℃的理由是 .
(2)第三步静置后析出NaHCO3晶体的原因是 ;用蒸馏水洗涤NaHCO3晶体的目的是除去杂质粒子 (用离子符号表示)。
(3)若向过滤所得母液中加入 (填写试剂名称),并作进一步处理,使NaCl溶液循环使用,同时可回收NH4Cl。
(4)纯碱产品不纯,含有NaHCO3、NaCl等杂质。测定纯碱中NaHCO3含量的方法是:准确称取纯碱样品Wg,放入锥形瓶中加蒸馏水溶解,加l-2滴酚酞指示剂,用物质的量浓度为cmol/L的盐酸滴定至溶液由红色到无色(指示CO32-+H+=HCO3-反应的终点), 所用盐酸体积为V1mL,再加1-2滴甲基橙指示剂,继续用盐酸滴定至溶液由黄变橙,所用盐酸总体积为V2mL。
① 实验室配制一定体积cmol/L盐酸需用的仪器除了容量瓶、烧杯、量筒外还需 ;在容量瓶的使用方法中,下列操作正确的是 (填写标号)
a.使用容量瓶前检验它是否漏水
b.容量瓶用蒸馏水洗净后,再用待配溶液润洗
c.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中.然后加蒸馏水定容
d.用容量瓶把溶液配制完成以后.直接贴上标签,放置备用
e.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手指托住瓶底,把容量瓶倒转和摇动几次
② 写出纯碱样品中NaHCO3质量分数的计算式:NaHCO3(%)= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com