
【题目】软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:

已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
金属离子 | Fe2+ | Fe3+ | Al3+ | Cu2+ | Mn2+ |
开始沉淀pH | 7.5 | 2.7 | 4.1 | 5.9 | 8.8 |
完全沉淀pH | 9.5 | 3.7 | 5.4 | 6.9 | 10.8 |
(1)提高浸出率的可采取的措施有____。
a.适当升高温度 b.搅拌 c.加适量纯碱 d.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是__________________________。
(3)调节pH为5.4~5.8的目的是______________。
(4)滤渣3的主要成分的化学式是_______。
(5)采用50℃碳化的原因是_________________________________。该过程发生反应的离子方程式是__________________。
(6)检验碳酸锰产品完全洗净的方法是_______________________________。
【答案】 ab MnO2+FeS2+2H2SO4![]() MnSO4+FeSO4+2S+2H2O 使Fe3+、Al3+完全沉淀 Cu(OH)2 温度过低反应太慢,过高,NH4HCO3会分解 2HCO3+Mn2+
MnSO4+FeSO4+2S+2H2O 使Fe3+、Al3+完全沉淀 Cu(OH)2 温度过低反应太慢,过高,NH4HCO3会分解 2HCO3+Mn2+![]() MnCO3↓+H2O+CO2↑ 取最后一次洗涤液,加入盐酸酸化的BaCl2溶液,若无沉淀,则已洗净
MnCO3↓+H2O+CO2↑ 取最后一次洗涤液,加入盐酸酸化的BaCl2溶液,若无沉淀,则已洗净
【解析】软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。根据流程图,硫酸与软锰矿和黄铁矿作用,二氧化锰与FeS2在酸性溶液中发生氧化还原反应,生成硫酸锰和硫沉淀,同时生成少量的硫酸铝、硫酸亚铁等,二氧化硅不反应,和硫一起形成滤渣Ⅰ;再加入二氧化锰,二氧化锰可将亚铁离子氧化为铁离子;加氨水调节溶液的pH=5.4~5.8把铁离子和铝离子转化为沉淀除去,则滤渣II为Fe(OH)3、Al(OH)3;继续加氨水调节溶液的pH=6~8把铜离子转化为沉淀除去,则滤渣Ⅲ为Cu(OH)2;加碳酸氢铵50℃碳化得碳酸锰、二氧化碳和硫酸铵等。
(1)为了提高锰元素的浸出率,在“浸取”时可采取的措施有:①适当升高温度;②搅拌;③加入足量硫酸增大硫酸浓度或粉粹矿石或延长浸泡时间,故选ab;
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,说明溶液中没有铁离子,则浸取时发生的主要反应的化学方程式为MnO2+FeS2+2H2SO4=MnSO4+FeSO4+2S+2H2O,故答案为:MnO2+FeS2+2H2SO4=MnSO4+FeSO4+2S+2H2O;
(3)根据上述分析,调节pH为5.4~5.8的目的是使Fe3+、Al3+完全沉淀,故答案为:使Fe3+、Al3+完全沉淀;
(4)滤渣3的主要成分为Cu(OH)2,故答案为:Cu(OH)2;
(5)温度过低反应太慢,过高,NH4HCO3会分解,因此采用50℃碳化,该过程发生反应的离子方程式为2HCO3+Mn2+=MnCO3↓+H2O+CO2↑,故答案为:温度过低反应太慢,过高,NH4HCO3会分解;2HCO3+Mn2+=MnCO3↓+H2O+CO2↑;
(6)根据流程图,碳酸锰上吸附有少量硫酸铵,检验碳酸锰产品是否洗净只需要检验硫酸根离子即可,故答案为:取最后一次洗涤液,加入盐酸酸化的BaCl2溶液,若无沉淀,则已洗净。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】[化学-选修5:有机化学基础]
甲苯在医药、农药,特别是香料合成中应用广泛,可合成以下物质:
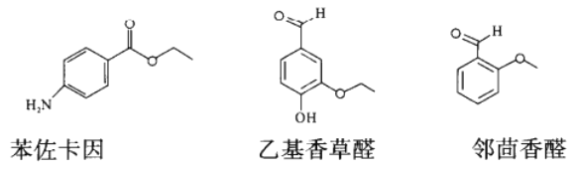
(1)苯佐卡因中含有的碱性官能团为____________(填名称)。
(2)乙基香草醛和邻茴香醛具有相同的亲水基团,该基团可用________(填物理方法)检测。
(3)写出符合下列条件的乙基香草醛的同分异构体的结构简式______(任写两种)。
a.苯环上连接两个互为对位的基团 b.有一个-CH3
c.与FeCl3溶液发生显色反应 d.能发生水解反应
(4)已知:
有机物M为含有两个互为邻位基团的芳香族化合物,且与本佐卡因互为同分异构,其合成路线如下:
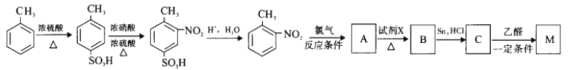
①生成A的“反应条件”为________;
②以上合成路线涉及的7个反应中,属于取代反应的有_________个;
③M的结构简式为___________;
④A→B反应的化学方程式为____________。
(5)参照上述合成路线,以甲苯和甲醇为原料(无机试剂任选),设计制备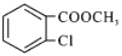 的合成路线___________。
的合成路线___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】孔雀石的主要成分为Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuCl2·3H2O及CaCO3的步骤如下:
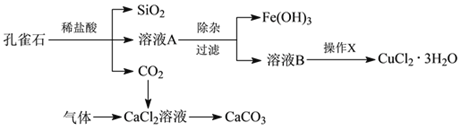
为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如下:
物质 | pH (开始沉淀) | pH(完全沉淀) |
Fe(OH)3 | 1.9 | 3.2 |
Fe(OH)2 | 7.0 | 9.0 |
Cu(OH)2 | 4.7 | 6.7 |
(1)在除杂过程时为了除去Fe2+,常加入绿色氧化剂,使Fe2+氧化为Fe3+,此过程涉及的离子方程式为________。
(2)然后再加入适当物质调节溶液的pH至_________ (填写范围),使Fe3+转化为Fe(OH)3,可以达到除去Fe3+,调整溶液pH不可选用下列中的________。
A.NaOH B.NH3·H2O C.CuO D.Cu(OH)2
(3)检验Fe(OH)3是否沉淀完全的实验方案是________________________。
(4)操作X包括________、________、过滤和洗涤等。CuCl2·3H2O加热灼烧的最终产物的化学式是 ______________。
(5)某种胃药片的治酸剂为CaCO3,该药片中CaCO3质量分数的测定步骤如下:
a.配制0.1mol·L-1的HCl溶液和0.1mol·L-1的NaOH溶液各250mL。
b.取0.6g磨碎后的胃药于锥形瓶中。
c.向锥形瓶内加入25.00mL 0.1 mol·L-1的HCl溶液。
d.以酚酞为指示剂,用0.1mol·L-1的NaOH溶液滴定,至达到滴定终点。
e.重复bcd三步的操作2次。
①读数时,若滴定前平视,滴定后仰视,则所测CaCO3的质量分数将________(选填“偏大”、“偏小”或“无影响”)。
②若滴定中NaOH溶液的平均用量为15.00mL,则胃药中碳酸钙的质量分数为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素在元素周期表中的位置为____________________
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 __________________
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4,反应生成N2和水蒸气。
已知①N2(g)=N2O4(l) △H1=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) △H2=-534.2kJ·mol-1
肼和N2O4反应的热化学方程式为___________________________
(4)“长征“火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,既能在短时间内产生巨大能量,产物又不污染空气( 产物都是空气成分)。将此原理设计为原电池,如下图所示,据此回答问题:
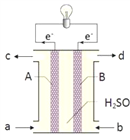
①B为___________极,从d口排出的气体是____________ 。
②A极发生的电极反应式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组需要用 18 mol/L 的浓硫酸配制80mL 3.0 mol/L 稀硫酸的实验步骤如下: ① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 稀释 ④ 检漏、 转移、洗涤 ⑤ 定容、摇匀 回答下列问题:
(1)所需浓硫酸的体积是________mL, 量取浓硫酸所用的量筒的规格是_________(用下列编号填空) 。
A.10 mL B.25 mL C.50 mL D.100 mL
(2)第⑤步实验的操作是继续向容量瓶中注入蒸馏水至离刻度线__________, 改用___________向容量瓶中滴加蒸馏水至___________为止。塞紧瓶塞,倒转摇匀并装试剂瓶。
(3)下列情况对所配制的稀硫酸浓度有何影响? (填 “ 偏大 ”“ 偏小 ” 或 “ 无影响”)
①所用的浓硫酸长时间放置在密封不好的容器中 ______________;
②容量瓶用蒸馏水洗涤后残留有少量的水_________________;
③在转入容量瓶前烧杯中溶液未冷却至室温_________;
④取完浓硫酸后洗涤量筒,并把洗涤液倒入烧杯___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容容器中,发生反应:2A(g)+B(s) ![]() C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( )
C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( )
①混合气体的密度不变
②混合气体的压强不变
③C(g)的物质的量浓度不变
④容器内A、C、D三种气体的浓度之比为2:1:1
⑤单位时间内生成n mol C,同时生成n mol D
⑥单位时间内生成n mol D,同时生成2n mol A
A. ①③⑤ B. ②③④ C. ①③⑥ D. ②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原子结构及元素周期律的知识,下列推断正确的是
A. ![]() 与
与![]() 得电子能力相同
得电子能力相同
B. 核外电子排布相同的微粒化学性质也相同
C. Cl-、 S2-、 Ca2+、 K+半径逐渐减小
D. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图表示的一些物质或概念间的从属关系中不正确的是( )
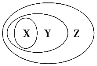
X | Y | Z | |
A | 氧化物 | 化合物 | 纯净物 |
B | 电解质 | 盐 | 化合物 |
C | 胶体 | 分散系 | 混合物 |
D | 含氧酸 | 酸 | 化合物 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com