
| A. | 加热蒸干NaCl、MgCl2溶液时可以得到晶体NaCl、MgCl2 | |
| B. | 相同条件下,等物质的量浓度的溶液导电能力:HCl>NH3•H2O | |
| C. | 溶液中离子结合质子(氢离子)的能力:C2O42->HC2O4->SO42- | |
| D. | 海洋封存CO2会导致局部海洋水体酸性增强,会破坏海洋生态环境 |
分析 A.MgCl2水解生成氢氧化镁和氯化氢,加热氯化氢挥发,最终得到的固体是氢氧化镁;
B.溶液的导电性强弱取决于溶液中离子浓度的大小;
C.对应的酸越强,则酸根离子得到质子的能力越弱;
D.二氧化碳与水反应生成碳酸,溶液呈酸性;
解答 解:A.MgCl2水解生成氢氧化镁和氯化氢,加热氯化氢挥发,最终得到的固体是氢氧化镁,得不到氯化镁,故A错误;
B.HCl是强电解质,NH3•H2O是弱电解质,相同条件下,等物质的量浓度的溶液中离子浓度:HCl>NH3•H2O,导电能力:HCl>NH3•H2O,故B正确;
C.酸性:HSO4->H2C2O4>HC2O4-,对应的酸越强,则酸根离子得到质子的能力越弱,则结合质子能力:C2O42->HC2O4->SO42-,故C正确;
D.二氧化碳与水反应生成碳酸,溶液呈酸性,会使海水酸性增强,破坏海洋生态环境,故D正确;
故选A.
点评 本题考查盐类的水解,侧重于学生的分析能力和基本理论知识的理解和运用的考查,注意把握盐类水解的原理和应用,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
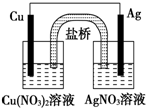
| A. | 将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同 | |
| B. | 该电池的负极反应为:Ag++e-═Ag | |
| C. | 在外电路中,电子由银电极流向铜电极 | |
| D. | 实验过程中取出盐桥,原电池仍继续工作 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
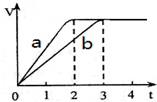 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图所示,下列说法正确的是( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图所示,下列说法正确的是( )| A. | 曲线a代表Al的反应过程,曲线b代表Mg的反应过程 | |
| B. | Mg和Al的质量之比为3:2 | |
| C. | Mg和Al的物质的量之比为3:2 | |
| D. | Mg和Al的反应速率之比为3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
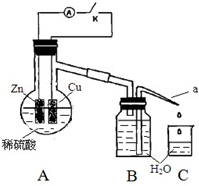 某同学分析Zn 与稀H2SO4的反应.
某同学分析Zn 与稀H2SO4的反应.| 1 分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1 分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 透闪石的化学式写成氧化物的形式为2CaO•5MgO•8SiO2•H2O | |
| B. | 透闪石中Mg的质量分数是Ca的质量分数的1.5倍 | |
| C. | 1molCa2Mg5Si8O22(OH)2与足量盐酸作用,至少需要14molHCl | |
| D. | 透闪石是一种新型无机非金属材料,难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com