
【题目】【加试题】乙酰苯胺具有解热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称,其制备原理如下:
已知:![]()
①苯胺易被氧化。
②乙酰苯胺、苯胺和醋酸的部分物理性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 溶解性 |
乙酰苯胺 | 114.3 | 305 | 微溶于冷水,易溶于热水 |
苯胺 | -6 | 184.4 | 微溶于水 |
醋酸 | 16.6 | 118 | 易溶于水 |
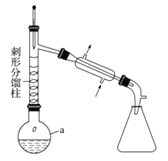
实验步骤如下:
步骤1:在a中,加入9mL (0.10 mol)苯胺、15 mL(0.27 mol)冰醋酸及少许锌粉,依照上图装置组装仪器。
步骤2:控制温度计读数在105℃左右,小火加热回流至反应完全。
步骤3:趁热将反应混合物倒入盛有100 mL 冷水的烧杯中,冷却后抽滤、洗涤,得到粗产品。
步骤4:将步骤3所得粗产品进一步提纯后,称得产品质量为10.8g。
请回答下列问题:
(1)仪器a的名称为 ,所选仪器a的最佳规格是 (填序号)。
A. 25 mL B.50 mL C.100 mL D.250 mL
(2)实验中加入少许锌粉的目的是 。
(3)步骤2中,控制温度计读数在105℃左右的原因是 。
(4)判断反应已基本完全的方法为 。
(5)步骤3中趁热将混合物倒入盛有冷水的烧杯中,“趁热”的原因是 。
(6)步骤4中粗产品进一步提纯,该提纯方法是 。
(7)本次实验的产率为 。
【答案】(1)圆底烧瓶 B
(2)防止苯胺被氧化,同时起着沸石的作用
(3)温度过低不能蒸出反应所生成的水或温度过高未反应的乙酸蒸出
(4)锥形瓶不再有水增加
(5)若让反应混合物冷却,则固体析出沾在瓶壁上不易处理
(6)重结晶
(7)80%
【解析】
试题分析:(1)根据装置图可知a仪器为圆底烧瓶;反应物液体的总体积超过22mL,由于圆底烧瓶所盛放的溶液体积一般不能超过![]() ,也不能低于
,也不能低于![]() ,因此最佳规格是50mL;
,因此最佳规格是50mL;
(2)苯胺易被氧化,加入锌粉,防止苯胺被氧化,同时起着沸石的作用,防止暴沸;
(3)已知醋酸的沸点为118℃,水的沸点为100℃,温度过高,未反应的乙酸会蒸出,降低反应物的利用率,温度过低,又不能除去反应生成的水,故选择控制温度计约105℃;
(4)反应生成水,水经过加热蒸发、冷凝进入锥形瓶中,若锥形瓶中水的量不再增加,说明反应基本完全;
(5)已知乙酰苯胺的熔点为114.3℃,常温下为固体,若让反应混合物冷却,则乙酰苯胺会以固体形式析出沾在瓶壁上不易处理,故需要“趁热”过滤;
(6)乙酰苯胺的溶解度受温度影响较大,且与乙酸、苯胺的溶解度相差较大,可以用重结晶的方法进行提纯;
(7)加入9mL (0.10mol)苯胺、15mL(0.27mol)冰醋酸及少许锌粉,所以乙酸过量,按照苯胺的物质的量计算,设生成的乙酰苯胺为xmol,![]() NH2+CH3COOH
NH2+CH3COOH![]()
![]() NHCOOCH3 +H2O
NHCOOCH3 +H2O
1mol 1mol
0.1mol x
则x=0.1mol,所以m(乙酰苯胺)=0.1mol×135g/mol=13.5g,
所以所得到乙酰苯胺的产率是![]() ×100%=80%;
×100%=80%;


科目:高中化学 来源: 题型:
【题目】甲醇可以补充和部分替代石油燃料,缓解能源紧张。利用CO可以合成甲醇。
(1)已知:CO(g)+![]() O(g)=CO2(g) △H1=-283.0kJ·mol-1
O(g)=CO2(g) △H1=-283.0kJ·mol-1
H2(g)+ ![]() O2(g)=H2O(l) △H2=-285.8kJ·mol-1
O2(g)=H2O(l) △H2=-285.8kJ·mol-1
CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(l) △H3=-764.5kJ·mol-1
O2(g)=CO2(g)+2H2O(l) △H3=-764.5kJ·mol-1
则CO(g)+2H2(g)=CH3OH(g) △H=__________kJ·mol-1
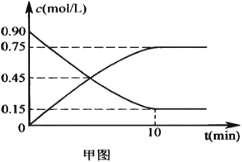
(2)甲图是反应时CO和CH3OH(g)的浓度随时间的变化情况。从反应开始到达平衡,用H2表示平均反应速率v(H2)=____________________。
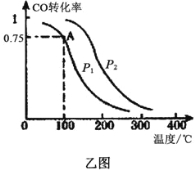
(3)一定条件下,在容积为VL的密闭容器中充入amolCO与2amolH2合成甲醇,平衡转化率与温度、压强的关系如乙图所示。
①P1__________P2(填“>”、“<”或“=”)
②该甲醇合成反应在A点的平衡常数K=__________(用a和V表示)
③下列措施中能够同时满足增大反应速率和提高CO转化率的是__________。(填写相应字母)
A.使用高效催化剂B.降低反应温度
C.增大体系压强D.不断将CH3OH从反应混合物中分离出来
E.向体系中再充入amolCO与2amolH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近研究用生物质原料合成高分子材料PET的流程如下:
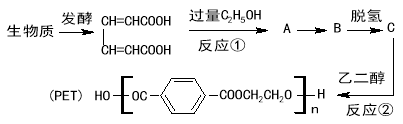
已知下列两个反应:
![]()
![]()
请回答下列问题:
(1)反应①属于 反应。
(2)PET的中文名称是 。
(3)有机物A、B的结构简式分别是 、 。
(4)写出反应②的化学方程式 。
(5)在有机物A的同分异构体F溶液中滴加氯化铁溶液显紫色。F的苯环上有四个取代基且一氯代物有只有一种,0.1molF 跟足量的金属钠反应,生成0.15mol氢气,F的核磁共振氢谱有4个吸收峰。试写出满足上述条件F的结构简式 (任写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修5:有机化学基础】
有机物A(C11H12O5)同时满足下列条件:①含苯环且不含甲基;②苯环上一氯取代物只有2种;③1 mol A与足量的NaHCO3反应生成1 mol CO2;④遇FeCl3溶液不显色。A有如图所示转化关系:

已知:
回答下列问题:
(1)A中有 种官能团,H的分子式为 。
(2)由C生成G的反应类型是 。
(3)G的结构简式为 ,K的结构简式为 。
(4)①写出C→D反应的化学方程式 ;
②写出I→J反应的离子方程式 。
(5)①C的同分异构体中能同时满足下列条件:a.能发生银镜反应,b.能发生皂化反应;c.能与Na反应产生H2气,共有 种(不含立体异构)。其中核磁共振氢谱显示为3组峰,且峰面积比为6﹕1﹕1的是 (写结构简式)。
②C的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是___________(填标号)。
A.元素分析仪 B.质谱仪 C.红外光谱仪 D.核磁共振仪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大。A、D同主族,可形成离子化合物X;B的氢化物与F的氢化物可反应生成离子化合物Y, 且B的单质是空气中含量最高的物质;C原子的最外层电子是次外层电子数的3倍;D、E、F 3种原子最外层共有11个电子, 且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水。
(1)B单质的结构式为 。
(2)用电子式表示化合物X的形成过程 。
(3)化合物Y的化学式为 ,A2C2的电子式为
(4)D、F最高价氧化物的水化物之间反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——物质结构与性质】
氮及其化合物与人类生产、生活息息相关。回答下列问题:
(1)基态N原子中电子在2p轨道上的排布遵循的原则是________。前4周期元素中,基态原子核外电子排布成单电子数最多的元素的价层电子排布式为__________________。
(2)C、N、O三种元素第一电离能从大到小的顺序是__________________________
(3)N2F2分子中N原子的杂化方式是___________________,l mol N2F2含有______mol![]() 键。
键。
(4)NF3的键角______NH3的键角(填“<”“>”或“=”),原因是__________________。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。l mol NH4BF4_________mol配位键。
(6)安全气囊的设计原理为6NaN3+FeIO3![]() Na2O+2Fe+9N2↑
Na2O+2Fe+9N2↑

①等电子体的原理是:原子总数相同,价电子总数相同的分子或离子具有相似的化学键特征,具有许多相近的性质。写出两种与N3-互为等电子体的分子或离子____________。
②Na2O的晶胞结构如图所示,品胞边长为566pm,晶胞中氧原子的配位数为_____,Na2O晶体的密度为_____g·cm-3(只要求列算式,不必计算出结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气在工业上有广泛用途。请回答以下问题:
(1)工业上利用N2(g)+3H2(g) ![]() 2NH3(g) H<0合成氨,某小组为了探究外界条件对该反应的影响,以c0 mol/L H2参加合成氨反应,在a、b两种条件下分别达到平衡,如图A。
2NH3(g) H<0合成氨,某小组为了探究外界条件对该反应的影响,以c0 mol/L H2参加合成氨反应,在a、b两种条件下分别达到平衡,如图A。
①相对a而言,b可能改变的条件是 ,判断的理由是__________________。
②a条件下,0~t0的平均反应速率v(N2)= mol·L-1·min-1。 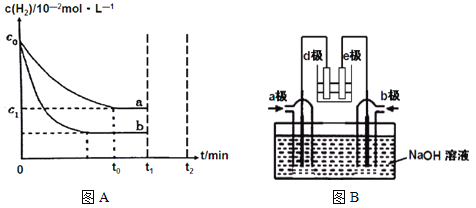
(2)有人利用NH3和NO2构成电池的方法,既能实现有效消除氮氧化物的排放减少环境污染,又能充分利用化学能进行粗铝的精炼,如图B所示,e极为精铝。
a极通入 气体(填化学式),判断的理由是___________________________________
(3)某小组往一恒温恒压容器充入9mol N2和23mol H2模拟合成氨反应,图C为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图。若体系在T2、60MPa下达到平衡。
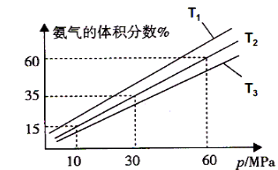
图C
①能判断N2(g)+3H2(g)![]() 2NH3(g)达到平衡的是______(填序号)。
2NH3(g)达到平衡的是______(填序号)。
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(N2)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②若T1、T2、T3温度下的平衡常数分别为K1、K2、K3,则K1、K2、K3由大到小的排序为 .
③此时N2的平衡分压为 MPa。(分压=总压×物质的量分数)
计算出此时的平衡常数Kp= 。(用平衡分压代替平衡浓度计算,结果保留2位有效数字并带上单位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石蜡油(主要是含17个碳原子以上的液态烷烃混合物)分解实验按照右图进行:
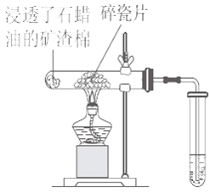
(1)石蜡油分解实验产生的气体的主要成分是 (填写序号)。
①只有甲烷 ②只有乙烯 ③烷烃跟烯烃的混合物。
(2)将石蜡油分解所得生成物通入到酸性高锰酸钾溶液中,现象是 。
(3)碎瓷片的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求回答下列问题:
(1)1-丁烯与溴水的反应 。
(2)相对分子质量为72的某烃,其一氯代物只有一种,则该烃的一氯代物的结构简式为_________。
(3)用系统命名方法命名下列有机化合物
(CH3)2CHCH(CH3)2_____________________________;
 ______________________________;
______________________________;
(4)已知结构式为 的物质互为同分异构体,我们称之为顺反异构。则分子式为C5H10的有机物,属于烯烃的同分异构体的数目为_________种(考虑顺反异构)。
的物质互为同分异构体,我们称之为顺反异构。则分子式为C5H10的有机物,属于烯烃的同分异构体的数目为_________种(考虑顺反异构)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com