
| A、干电池的负极是锌筒 |
| B、MnO2在碳棒上发生还原反应 |
| C、闲置时间过长干电池也会失去供电能力 |
| D、工作时电解液中的NH4+移向负极 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、22.4LSO2与0.5molO2混合催化氧化,生成NA个SO3分子 |
| B、1mol乙炔在空气中燃烧,一定生成2NA个CO2分子 |
| C、1molCl2与1molCH4恰好完全反应,则转移的电子总数为2NA |
D、 11g某硫化磷(如图)中含P-S键数目为0.45NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知:X、Y、Z、W都是周期表中前四周期的元素,它们的核电荷数依次增大.X的简单阴离子最外层有2个电子,Y原子最外层电子数是内层电子数的两倍,Z的原子序数是Y的两倍,在元素周期表中W元素位于第11列.
已知:X、Y、Z、W都是周期表中前四周期的元素,它们的核电荷数依次增大.X的简单阴离子最外层有2个电子,Y原子最外层电子数是内层电子数的两倍,Z的原子序数是Y的两倍,在元素周期表中W元素位于第11列.查看答案和解析>>
科目:高中化学 来源: 题型:
 如图为相互串联的甲、乙两电解池.试回答:
如图为相互串联的甲、乙两电解池.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | ||
| C | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液中由水电离出的c(H+)=1×10-3mol?L-1 |
| B、pH=2的HA溶液与pH=3的HCl溶液:c(HA)=10 c(HCl) |
| C、pH=3的HA溶液与pH=11的NaOH溶液等体积混合后所得的溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) |
| D、0.1mol?L-1HA溶液与0.05mol?L-1NaOH溶液等体积混合后所得的溶液中:c(A-)+c(HA)=0.05mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、S2-、K+、NO3- |
| B、NH4+、NO3-、Al3+、K+ |
| C、MnO4-、K+、CO32-、Na+ |
| D、K+、SO42-、HCO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、用铂作电极电解MgCl2溶液:2Cl-+2H2O
| ||||
B、用石墨电极电解氯化铜溶液:Cu2++2Cl-+2H2O
| ||||
C、向Ca(HCO3)2溶液中滴加少量的NaOH溶液:Ca2++HC
| ||||
| D、将少量氯气通入溴化亚铁溶液中:2Br-+Cl2═Br2+2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
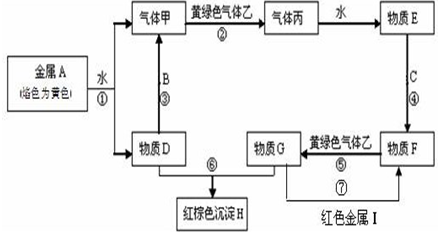 现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,金属A的焰色为黄色,金属B既能跟酸又能跟强碱反应,金属C在地壳中的含量居第四位.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,金属A的焰色为黄色,金属B既能跟酸又能跟强碱反应,金属C在地壳中的含量居第四位.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com