
【题目】某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
探究浓度对醋酸电离程度的影响
用pH计测定25 ℃时不同浓度的醋酸的pH,其结果如下:
醋酸浓度/(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
回答下列问题:
(1)写出醋酸的电离方程式:___________________________________________。
(2)醋酸溶液中存在的微粒有________________________________________。
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是________________________________________________________________________。
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度将(填“增大”、“减小”或“不变”)__________。
【答案】(1)CH3COOH![]() CH3COO-+H+
CH3COO-+H+
(2)H+;CH3COO-;CH3COOH;OH-
(3)合理答案均可得分
(4)增大
【解析】
试题分析:(1)醋酸是弱电解质,在水溶液里部分电离生成醋酸根离子和氢离子,电离方程式为:CH3COOH![]() CH3COO-+H+。
CH3COO-+H+。
故答案为:CH3COOH![]() CH3COO-+H+;
CH3COO-+H+;
(2)醋酸的电离方程式为CH3COOHCH3COO-+H+,则溶液中存在的微粒有:H2O、
CH3COOH、CH3COO-、H+、OH-。
故答案为:H2O、CH3COOH、CH3COO-、H+、OH-;
(3)当醋酸浓度为0.001mol/L 时,溶液中的氢离子浓度小于0.001mol/L,说明醋酸部
分电离为弱电解质。
故答案为:当醋酸浓度为0.001mol/L 时,溶液中的氢离子浓度小于0.001mol/L;
(4)根据表中数据知,醋酸为0.0100mol/L,溶液的pH3.38,醋酸为0.0010mol/L,溶液的pH为3.88,所以醋酸浓度越小,醋酸的电离程度增大。
故答案为:增大。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】关于下列各实验装置图的叙述中,正确的是
A.装置①可用于分离碘和氯化钠的固体混合物
B.装置②可用于吸收HCl或NH3
C.装置③可用于分解NH4HCO3制备NH3
D.装置④的b口进气可收集CO2或NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期原子序数依次递增的A、B、C、D、E、F六种元素,已知B原子最外层电子数是A原子次外层电子数的3倍,是D原子最外层电子数的2倍;C原子内层电子总数是最外层电子数10倍;A、B、D三种元素的原子最外层电子数之和为13;A和B原子最外层电子数之和与D和F原子最外层电子数之和相等;D和E是相邻两种元素。回答下列问题:
(1)E元素的名称: ;其在元素周期表中的位置是 。
(2)AB2的结构式 ;B的氢化物中原子个数比1:1化合物的电子式 。
(3)A和E元素的最高价含氧酸的酸性较强的是 ;(填化学式)
(4)B、C、D、F四种元素原子半径由大到小的顺序是 (填元素符号),离子半径最小的是 (填离子符号)。
(5)A、B、C三种元素组成原子个数比为nA:nB:nC=1:3:2的化合物,将足量AB2通入该化合物溶液中反应的离子方程式是 。
(6)短周期元素M与D元素位于不同主族,根据对角线规则二者某些性质相似。将M的最高价氧化物溶于C的最高价氧化物对应的水化物溶液中,发生反应的离子方程式为 。
(7)E和F形成的化合物X在高温条件下可以被氢气还原,工业上常用此反应制取高纯度的单质E,写出该化学反应的方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯仿(CHCl3)常用作有机溶剂和麻醉剂,常温下在空气中易被氧化。实验室中可用热还原CCl4法制备氯仿,装置示意图及有关数据如下:
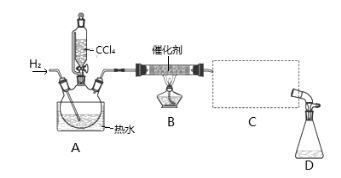
物质 | 相对分子质量 | 密度/(g·mL-1) | 沸点/℃ | 水中溶解性 |
CHCl3 | 119.5 | 1.50 | 61.3 | 难溶 |
CCl4 | 154 | 1.59 | 76.7 | 难溶 |
实验步骤:
①检验装置气密性;②开始通入H2; ③点燃B处酒精灯;
④向A处水槽中加入热水,接通C处冷凝装置的冷水; ⑤向三颈瓶中滴入20 mLCCl4;
⑥反应结束后,停止加热,将D处锥形瓶中收集到的液体分别用适量NaHCO3溶液和水洗涤,分出的产物加入少量无水CaCl2固体,静置后过滤;
⑦对滤液进行蒸馏纯化,得到氯仿15 g。请回答:
(1)若步骤②和步骤③的顺序颠倒,则实验中产生的不良后果可能为 。
(2)B处中发生主要反应的化学方程式为 。
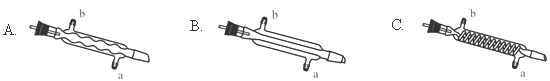
(3)C处中应选用的冷凝管为 (填选项字母);冷水应从该冷凝管的 (填“a”或“b”)口接入。
(4)步骤⑥中,用水洗涤的目的为 。
(5)该实验中,氯仿的产率为 。
(6)氯仿在空气中能被氧气氧化生成HCl和光气(COCl2),该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,发生如下反应:N2(g)+3H2(g) ![]() 2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0 mol和6.0 mol,2min后反应达到平衡,平衡时NH3的物质的量与H2的物质的量相等,已知容器的容积为5.0 L且不可变,试回答下列问题:
2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0 mol和6.0 mol,2min后反应达到平衡,平衡时NH3的物质的量与H2的物质的量相等,已知容器的容积为5.0 L且不可变,试回答下列问题:
(1) 其达到平衡状态的标志是____________________。
①氨的生成速率与氨的分解速率相等
②断开1个N≡N键的同时有6个N—H键生成
③N2、H2、NH3的体积分数不再变化
④气体的总压强不变
⑤N2、H2、NH3分子数之比为1:3:2
⑥N2、H2和NH3的浓度相等
⑦v(N2)=1/3v(H2)
⑧v正(N2)=1/3v逆(H2)
⑨混合物的密度不变
⑩混合物的平均相对分子质量不变
A.①③④⑤⑦⑩ B.①③④⑧⑩
C.①③④⑤⑧⑩ D.全部
(2)从反应开始到达到平衡用N2表示该反应的速率为: mol·L-1·min-1。
(3)平衡时H2的物质的量浓度为 mol·L-1。
(4)H2的转化率是____________。
(5)平衡时混合气体中NH3的体积分数是_______%(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将过量的CO2分别通入①CaCl2溶液,②Na2SiO3溶液,③Ca(ClO)2溶液,④饱和Na2CO3溶液,最终有沉淀析出的是( )
A. ①②③④ B. ②④ C. ①②③ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表中所列字母分别代表一种元素。

(1)G的气态氢化物比J的气态氢化物 (填“稳定”或“不稳定”,此空1分)。
(2)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为________;该物质溶于水后的溶液呈________性(填“酸”、“碱”或“中”)。
(3)元素C和H的最高价氧化物对应的水化物相互反应的离子方程式为: 。
(4)元素G和L的原子序数相差: ,它们的氢化物的水溶液酸性相对强的是: (填化学式)
(5)表中A和F两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为:
A.MnO2B.Na2SO4C.FeCl3D.KMnO4
(6)K为生产、生活中应用最广泛的金属,通常采用的冶炼方法为:
A.电解法 B.热分解法 C.热还原法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知2 mol氢气燃烧生成液态水时放出572 kJ热量,反应方程式是
2H2(g)+O2(g)==2H2O(l)
(l)请回答下列问题:
①该反应的生成物能量总和________(填“大于”、“小于”或“等于”)反应物能量总和。
②若2 mol氢气完全燃烧生成水蒸气,则放出的热量________(填“>”、“<”或“=”)572 kJ。
③与化石燃料相比,利用氢能源有很多优点,请说出其中一点______________________。
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g)![]() 2SO3(g) ΔH1=-197 kJ·mol-1;
2SO3(g) ΔH1=-197 kJ·mol-1;
H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l)ΔH3=-545 kJ·mol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是_________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com