
【题目】元素R,X,T,Z,Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( ) 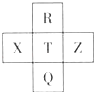
A.非金属性:Z<T<X
B.R与Q原子核外电子数相差26
C.气态氢化物稳定性:R<T<Q
D.最高价氧化物的水化物的酸性:X>T
科目:高中化学 来源: 题型:
【题目】用乙炔为原料制取CHClBr—CH2Br,下列方法中最可行的是( )
A.先与HBr加成后再与HCl加成
B.先与H2完全加成后再与Cl2、Br2取代
C.先与HCl加成后再与Br2加成
D.先与Cl2加成后再与HBr加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应. 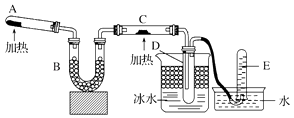
回答下列问题:
(1)A中加入的物质是 , 发生反应的化学方程式是;
(2)B中加入的物质是 , 其作用是;
(3)实验时在C中发生反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下的HCl气体4.48L溶于水形成100ml溶液,然后与足量的铁屑充分反应.计算:
(1)所得盐酸的物质的量浓度;
(2)生成H2的体积;
(3)将生成的FeCl2配成400ml溶液,此溶液中FeCl2的物质的量浓度是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氯气用导管通入较浓的NaOH和H2O2的混和液中,在导管口与混和液的接触处有闪烁的红光出现.这是因为通气后混和液中产生的ClO﹣被H2O2还原,发生激烈反应,产生能量较高的氧分子,然后立即转变为普通氧分子,多余的能量以红光放出.本实验所用的仪器及导管如图1所示. 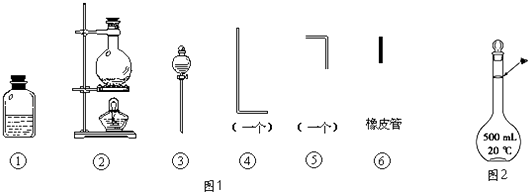
根据要求填写下列空白:
(1)组装氯气发生装置时,应选用的仪器及导管为(填写图中编号).
(2)本实验进行时,按气流方向从左到右的顺序,气体流经的各仪器及导管的编号依次为 .
(3)仪器①的橡皮塞上至少应有2个孔的原因是 .
(4)本实验需配置10molL﹣1的NaOH溶液500mL,用到的仪器除了托盘天平、烧杯外,还须用到的仪器有(填仪器名称),定容时操作如图2,则所配溶液浓度(填“偏高”或“偏低”).
(5)实验时仪器①中ClO﹣与H2O2反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CH4和CO组成的混合气体,在标准状况下的密度为1gL﹣1 , 则混合气体中CH4和CO的质量比为( )
A.1:1
B.1:2
C.2:3
D.7:8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)是一种高能燃料,在工业生产中用途广泛.
(1)写出肼的电子式 , 1mol N2H4中有个极性共价键.
(2)NH3与NaClO反应可以得到肼,该反应的化学方程式为 .
(3)发射火箭时,肼(N2H4)为燃料,双氧水作氧化剂,两者反应生成氮气和气态水.已知1.6g液态N2H4在上述反应中放出64.22kJ的热量,写出该反应的热化学方程式: .
(4)肼﹣空气燃料电池是一种碱性电池,该电池放电时负极反应式为 .
(5)肼性质与氨气相似,易溶于水,可发生如下电离过程:Ⅰ、N2H4+H2O═N2H5++OH﹣Ⅱ、N2H5++H2O═N2H62++OH﹣
①常温下,某浓度N2H6C12溶液的pH为5,则该溶液中由水电离产生的c(OH﹣)= .
②已知在相同条件下过程I的进行程度大于N2H5+的水解程度.常温下,若0.2mol/L N2H4溶液与0.1mol/L HCl溶液等体积混合,则溶液中N2H5+、N2H4H2O、Cl﹣、OH﹣、H+ 粒子浓度由大到小的顺序为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质量相等的SO2 和SO3,物质的量之比为_________, 硫原子个数之比为______,氧原子的原子个数之比为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com