

| �¶�/�ܽ��/�� | 0�� | 10�� | 20�� | 30�� | 40�� | 50�� |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
���� ��1��Aװ�����Ʊ�������̼�����װ�ã���̼��ƺ����ᷢ����Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼��Cװ��ϡ������β������װ�����չ����İ�����
��2��Bװ���е��Թ��������а����Ȼ��Ƶı�����Һ��ͨ�������̼����ᷢ����Ӧ����̼�����ƺ��Ȼ�泥��¶�Խ��Խ������̼�����Ƶľ���������
��3��ͨ�������̼û�еõ�̼�����ƾ��壬�Ƕ�����̼�����к����Ȼ������壬ͨ���Ͱ�����Ӧ��������̼�����ƣ�������Ҫ��һ��ϴ��װ���ñ���̼��������Һ��ȥ������̼�е��Ȼ������壻
��4��̼���������ȷֽ�Ϊ̼���ơ�ˮ��������̼��̼��������ȷֽ�Ϊ������ˮ��������̼��̼���������ᷴӦ�������壬�Դ����ʵ�飻
��5�����NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3������������̼�����Ƶ����������ʵ�����ɵ�̼�����Ƶ�����������ʣ�
��� �⣺��1��Aװ������ȡ������̼�����װ�ã���̼��ƺ����ᷢ����Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼����Ӧ�����ӷ���ʽΪ��CaCO3+2H+=Ca2++CO2��+H2O��Cװ��ϡ������β������װ�����չ����İ�������ֹ��Ⱦ������
�ʴ�Ϊ��CaCO3+2H+=Ca2++CO2��+H2O�����մ�Bװ���е��Թ����ݳ��İ��������ٶԻ�������Ⱦ��
��2��Bװ���е��Թ��������а����Ȼ��Ƶı�����Һ��ͨ�������̼����ᷢ����Ӧ����̼�����ƺ��Ȼ�泥�����ͼ�������֪�¶�Խ�ͣ�̼�����Ƶ��ܽ��ԽС�������¶�Խ��Խ������̼�����Ƶľ���������
�ʴ�Ϊ���¶�Խ��̼�������ܽ��ԽС������������
��3��������̼�����к����Ȼ������壬ͨ���Ͱ�����Ӧ��������̼�����ƣ����ԵIJ���̼�����ƾ��壬������Ҫ��A��B֮���һ��ϴ��װ���ñ���̼��������Һ��ȥ������̼�е��Ȼ������壬
�ʴ�Ϊ��A��B������NaHCO3��Һ����ȥCO2�л��е�HCl���壻
��4��̼�������ڼ��ȵ�����������̼���ơ�ˮ�Ͷ�����̼����ӦΪ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2�����а�ɫ����̼����ʣ�̼࣬����泥�NH4HCO3�����ȷֽ⣬���ɰ�����NH3����������̼��ˮ����Ӧ�Ļ�ѧ����ʽΪ��NH4HCO3$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+CO2��+H2O������ʣ�࣬�����жϸþ�����̼�����ƾ��������̼����茶��壬����Ϊ��ȡ�������������Թ��У��ھƾ����ϼ���ʹ���ַ�Ӧ���а�ɫ����ʣ�࣬���岻��NH4HCO3�����Թ���ȴ����ʣ������м����������ᣬ����Ӧ�������������ݣ�������NaHCO3��������ʳ�Σ�
�ʴ�Ϊ��ȡ�������������Թ��У��ھƾ����ϼ���ʹ���ַ�Ӧ���а�ɫ����ʣ�࣬���岻��NH4HCO3���Ҵ��Թ���ȴ����ʣ������м����������ᣬ����Ӧ�������������ݣ�������NaHCO3��������ʳ�Σ�
��5������ʳ��ˮ�к�NaCl������Ϊ5.85g��������������̼������Ϊxg��
NH3+CO2+NaCl+H2O�TNH4Cl+NaHCO3�����壩��
58.5 84
5.85g x
x=$\frac{84��5.85g}{58.5}$=8.4g��
ʵ���õ������NaHCO3���������Ϊ5.4g��
��̼�����ƵIJ���Ϊ$\frac{5.04g}{8.4g}$��100%=60%��
�ʴ�Ϊ��60%��
���� ���⿼�����ʵ��Ʊ�ʵ�飬Ϊ��Ƶ���㣬�����Ʊ�ʵ��ԭ����ʵ��װ�õ����á����ʵ�����Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��ʵ��������������ݷ�������������ѵ������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3VB���棩=2VC������ | |
| B�� | �����������ƽ��Ħ���������ٱ仯 | |
| C�� | ��λʱ������nmolA��ͬʱ����3nmolB | |
| D�� | ������������ܶȲ��ٱ仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �ۢܢ� | C�� | �ۢ� | D�� | �٢ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����NA����ԭ�ӵĺ����ڱ�״���µ����ԼΪ11.2 L | |
| B�� | 1.7 g NH3���еĵ�����ΪNA | |
| C�� | ��״���£�11.2 LH2O���еķ�����Ϊ0.5 NA | |
| D�� | 22.4 L�������еķ�����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
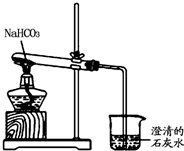 Na2CO3��NaHCO3�����ֳ��������Σ�
Na2CO3��NaHCO3�����ֳ��������Σ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ƭ��ϡ���ᷴӦ | B�� | ���ȵ�̿�������̼��Ӧ | ||
| C�� | �����������Ȼ�立�Ӧ | D�� | ������������Ʒ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �ڢۢܢ� | D�� | �٢ڢۢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com