
��
BaSΪԭ���Ʊ�Ba(OH)2��8H2O�Ĺ����ǣ�BaS��HCl��Ӧ��������Һ��70�桫90��ʱ�����NaOH��Һ���ã����ӣ���ȴ��õ�Ba(OH)2��8H2O���壮�����±���������Ч�ʸߡ��ɱ��͵�Ba(OH)2��8H2O������·�����ʹBaS��CuO��Ӧ����(1)д���·����ķ�Ӧ����ʽ________��
(2)�÷�Ӧ�ķ�Ӧ��CuO�Dz����Ϊʲô�÷�Ӧ���ܽ��У�________��
(3)�����·�������Ч�ʸߡ��ɱ��͵�ԭ��________��
 ������ÿ�ʱ��ҵϵ�д�
������ÿ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ||
| ||
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014���Ĵ�ʡ�����и�����һ���¿����ۻ�ѧ�Ծ��������棩 ���ͣ������
����Na����Ba2����Cu2����SO42����Cl������γɵ�����ǿ�������Һ���ֱ�װ����ͼװ���еļס��ҡ��������ձ��н��е�⣬�缫��Ϊʯī�缫��
��ͨ��Դ������һ��ʱ��������c�缫�������ӡ������¸��ձ�����ҺpH����ʱ��t�Ĺ�ϵ������ͼ�������������ܽ������Ӱ�죩���ݴ˻ش��������⣺

��1���ڼ����ձ��еμӷ�̪�� ������a��b��������Һ���졣
��2��д�����ձ��з�����Ӧ�Ļ�ѧ����ʽ ��
��3���缫f�Ϸ����ĵ缫��ӦʽΪ ��
��4��������һ��ʱ�������ձ���c�缫����������8g��Ҫʹ���ձ�����Һ�ָ���ԭ����״̬��Ӧ���еIJ����� ��
��ҵ������BaSO4�Ʊ�BaCl2�Ĺ����������£�
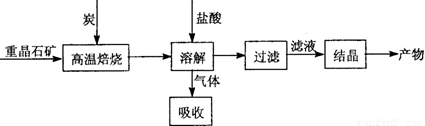
ij�С���ͬѧ��ʵ�������ؾ�ʯ����Ҫ�ɷ�BaSO4��Ϊԭ�ϣ��������������̽���ģ��ʵ�顣
��1�����������У������ù���NaOH��Һ���յõ�Na2S��Na2Sˮ��Һ�Լ��Ե�ԭ���� ���������ӷ���ʽ��ʾ��
��2����֪�йط�Ӧ���Ȼ�ѧ����ʽ���£�
BaSO4(s) +4C(s) 4CO(g)+BaS(s)
��H1 =
+571.2kJ/mol ��
4CO(g)+BaS(s)
��H1 =
+571.2kJ/mol ��
C(s) +CO2(g) 2CO(g)
��H2 =
+172.5kJ/mol
��
2CO(g)
��H2 =
+172.5kJ/mol
��
��ӦBaSO4(s)
+2C(s) 2CO2(g)
+ BaS(s) ��H3 =
2CO2(g)
+ BaS(s) ��H3 =
��3���ڸ��±����ؾ�ʯ�����б�����������̿��ͬʱ��Ҫͨ���������Ŀ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�걱���в�ƽ��������ѧ����ĩ�������ۻ�ѧ�Ծ��������棩 ���ͣ������
�������������������й㷺Ӧ�á�
��ҵ�����ؾ�ʯ����Ҫ�ɷ�BaSO4��Ϊԭ���Ʊ�BaCl2���乤������ʾ��ͼ���£�
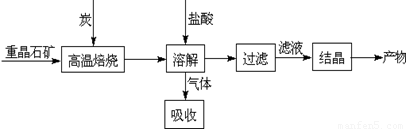
ij�о�С��������ϵã�
BaSO4��s��+4C��s�� 4CO��g��+BaS��s����H1=+571.2kJ•mol-1
��
4CO��g��+BaS��s����H1=+571.2kJ•mol-1
��
BaSO4��s��+2C��s�� 2CO2��g��+BaS��s����H2=+226.2kJ•mol-1
��
2CO2��g��+BaS��s����H2=+226.2kJ•mol-1
��
��1���ù���NaOH��Һ�������壬�õ����ơ��÷�Ӧ�����ӷ���ʽ�� ��
��2����ӦC��s��+CO2��g�� 2CO��g���ġ�H= ��
2CO��g���ġ�H= ��
��3��ʵ�������б�����������̿��ͬʱ��Ҫͨ���������Ŀ��������
�ٴ�ԭ�ϽǶȿ��� ��
�ڴ������Ƕȿ����٢�Ϊ���ȷ�Ӧ��̿��������Ӧ����ά�ַ�Ӧ������¡�
��4����С��ͬѧ���BaSO4��ˮ�еij����ܽ�ƽ������һ���о��������Ϸ�����ij�¶�ʱBaSO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ��
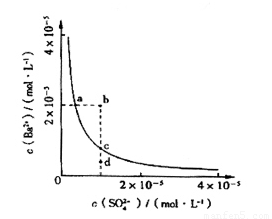
��С��ͬѧ����������ֹ۵㣺
�ٵ�����SO42-����Һ�м���Ba2+ ʹSO42-������ȫ�����ʱSO42-����Һ�е�Ũ��Ϊ0
�ڼ���Na2SO4����ʹ��Һ��a��䵽b��
��ͨ����������ʹ��Һ��d��䵽c��
��d����BaSO4��������
������ȷ���� ������ţ���
��ijȼ�ϵ����CaHSO4����Ϊ����ʴ���H+��������ṹ��ͼ��ʾ������ܷ�Ӧ�ɱ�ʾΪ2H2+O2�T2H2O��
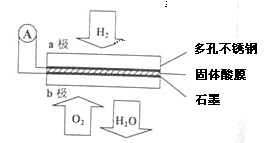
��ش�
��5��H+�� ��ͨ�����������ʴ��ݵ���һ������a����b����
��6��b���Ϸ����ĵ缫��Ӧ�� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com