
分析 (1)盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,要先加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除过量的钡离子;
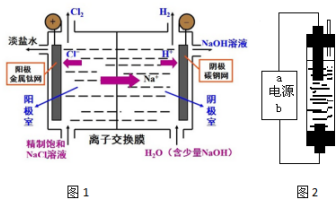
(2)电解NaCl溶液时,水电离出来的氢离子在阴极反应,阳极上氯离子放电生成氯气;
(3)阴极电极反应式为 2H++2e-→H2↑,生成11.2L氢气消耗1mol氢离子,溶液中生成1mol氢氧根离子,据此分析;
(4)若采用无隔膜电解食盐水,Cl2和NaOH充分接触,产物仅是NaClO和H2,则阳极上氯离子放电生成次氯酸钠、阴极上氢离子放电,据此分析解答;
(5)NaClO是弱酸强碱盐,其水解导致溶液显碱性.
解答 解:(1)要先除硫酸根离子,然后再除钙离子,Na2CO3可以除去过量的钡离子,否则过量的钡离子不能完全除尽,至于加NaOH除去镁离子顺序不受限制,可放在加入BaCl2之前或之后,因为过量的NaOH加HCl就可以调节了,只要将三种离子完全除去,过滤即可,最后加HCl除去过量的氢氧根离子碳酸根离子,故答案为:bac;(2)电解NaCl溶液时,水电离出来的氢离子在阴极反应,促进了水的电离,阳极上氯离子放电生成氯气,电极反应式为 2Cl--2e-→Cl2↑,
故答案为:促进; 2Cl--2e-→Cl2↑;
(3)阴极电极反应式为 2H++2e-→H2↑,生成11.2L氢气即0.5mol氢气,消耗1mol氢离子,溶液中生成1mol氢氧根离子,所以pH升高,c(OH-)=$\frac{1mol}{10L}$=0.1mol/L,
故答案为:升高;0.1mol/L;
(4)若采用无隔膜电解食盐水,Cl2和NaOH充分接触,产物仅是NaClO和H2,则阳极上氯离子放电生成次氯酸钠、阴极上氢离子放电,电池反应式为NaCl+H2O$\frac{\underline{\;通电\;}}{\;}$NaClO+H2↑,故答案为:NaCl+H2O$\frac{\underline{\;通电\;}}{\;}$NaClO+H2↑;
(5)NaClO是弱酸强碱盐,其水解导致溶液显碱性,水解方程式为ClO-+H2O?HClO+OH-,故答案为:ClO-+H2O?HClO+OH-.
点评 本题考查原电池和电解池原理、电极反应式的书写、盐类水解,明确电极上得失电子及反应物质是解本题关键,电极反应式的书写是学习难点,要注意结合电解质溶液的酸碱性书写,难度中等.


科目:高中化学 来源: 题型:实验题
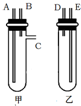 某兴趣小组要进行有关氢气的定量测定实验,为保证氢气不损失,设计用甲、乙两装置及橡胶管完成锌粒和稀硫酸制取氢气的操作.步骤如下:
某兴趣小组要进行有关氢气的定量测定实验,为保证氢气不损失,设计用甲、乙两装置及橡胶管完成锌粒和稀硫酸制取氢气的操作.步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2与O5 | |
| B. | 1H和2H | |
| C. | 淀粉和纤维素 | |
| D. | CH3-CH2-CH2-CH3与 CH3-CH (CH3)-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验描述 |
| A | 将SO2通入到紫色石蕊溶液中,溶液先变红后褪色 |
| B | 将SO2通入到KMnO4(H+)溶液中,紫色褪去 |
| C | 将Cl2与SO2 按物质的量之比1:1混合后,通入到品红溶液中,红色褪去 |
| D | 将CO2通入BaCl2溶液,出现白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C3H5O | B. | C2H8N2 | C. | C2H8 | D. | C2H5N |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性氧化物一定是非金属氧化物 | B. | 碱性氧化物一定是金属氧化物 | ||
| C. | 氧气和臭氧是氧元素的不同核素 | D. | H2 D2 T2 互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
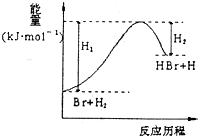
| A. | 正反应为吸热反应 | |
| B. | 加人催化剂,该化学反应的反应热改变 | |
| C. | 反应物总能量高于生成物总总量 | |
| D. | 升高温度可增大正反应速率,降低逆反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com