
FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
|
| A. | 加入KSCN溶液一定不变红色 | B. | 溶液中一定含Fe2+ |
|
| C. | 溶液中一定不含Cu2+ | D. | 剩余固体中一定含Cu |
| 铁的化学性质.. | |
| 专题: | 元素及其化合物. |
| 分析: | FeCl3、CuCl2的混合溶液中加入铁粉,Fe先和FeCl3反应生成FeCl2,然后Fe再和CuCl2发生置换反应生成FeCl2、Cu,如果充分反应后仍有固体存在,如果固体是Fe和Cu,则溶液中溶质为FeCl2,如果溶液中固体为Cu,则溶液中溶质为FeCl2或FeCl2和CuCl2,据此分析解答. |
| 解答: | 解:FeCl3、CuCl2的混合溶液中加入铁粉,Fe先和FeCl3反应生成FeCl2,然后Fe再和CuCl2发生置换反应生成FeCl2、Cu,如果充分反应后仍有固体存在,如果固体是Fe和Cu,则溶液中溶质为FeCl2,如果溶液中固体为Cu,则溶液中溶质为FeCl2或FeCl2和CuCl2, A.溶液中溶质一定没有Fe3+,所以加入KSCN溶液一定不变红色,故A正确; B.根据以上分析知,溶液中一定含有Fe2+,可能含有Cu2+,故B正确; C.根据以上分析知,溶液中可能含有Cu2+,故C错误; D.Fe的还原性大于Cu,所以固体中一定含有Cu,故D正确; 故选C. |
| 点评: | 本题考查金属的性质,明确离子、金属反应先后顺序是解本题关键,根据固体成分确定溶液中溶质成分,侧重考查分析能力,题目难度中等. |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
同周期元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4︰3,Z原子比X原子的核外电子数多4。下列说法正确的是 ( )
A. W、Y、Z的电负性大小顺序一定是Z>Y>W
B. W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z
C.Y、Z形成的分子的空间构型可能是正四面体
D.WY2分子中σ键与π键的数目之比是2︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:P4(s)+6Cl2(g)=4PCl3(g) ΔH=akJ·mol-1
P4(s)+10Cl2(g)=4PCl5(g) ΔH= bkJ·mol-1
P4具有正四面体结构,PCl5中P-Cl键的键能为ckJ·mol-1,PCl3中P-Cl键的键能为1.2ckJ·mol-1
下列叙述正确的是( )
A.P-P键的键能大于P-Cl键的键能
B.可求Cl2(g)+PCl3(g)=PCl5(s)的反应热ΔH
C.Cl-Cl键的键能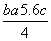 kJ·mol-1
kJ·mol-1
D.P-P键的键能为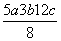 kJ·mol-1
kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在工业生产和日常生活中有着重要的应用.下列说法正确的是( )
|
| A. | 陶瓷、水泥和光导纤维均属于硅酸盐材料 |
|
| B. | Na2O2、H2O2所含化学键完全相同,都能作供氧剂 |
|
| C. | 常温下,浓硫酸、浓硝酸与铝均能发生钝化,均能用铝罐储运 |
|
| D. | NaClO和明矾都能作消毒剂或净水剂,加入酚酞试液均显红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应①、②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4═2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是( )
|
| A. | 两个反应中均为硫元素被氧化 |
|
| B. | 碘元素在反应①中被还原,在反应②中被氧化 |
|
| C. | 氧化性:Mn02>SO42﹣>I03﹣>I2 |
|
| D. | 反应①、②中生成等量的I2时转移电子数比为1:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能达到相应目的是( )
|
| A. |
制备少量的氧气 |
|
| B. |
证明氧化性Cl2>Br2>I2 |
|
| C. |
将海带灼烧成灰 |
|
| D. |
说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可用MnO2和KClO3混合加热的方法制取氧气:现有下列仪器或装置:
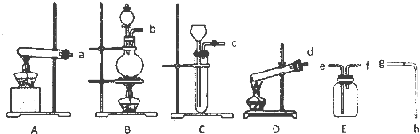
(1)A﹣D装置中,用作KClO3为原料制氧气的反应装置是 (填序号).
(2)排水法收集氧气,接口顺序是:氧气出口→ → →g→h→烧杯(填序号).
查看答案和解析>>
科目:高中化学 来源: 题型:
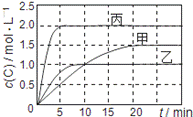
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 1L | 1L | 2L |
| 温度 | T1 | T2 | T2 |
| 反应物 起始量 | 1molA 2molB | 1molA 2molB | 4molA 8molB |
下列说法正确的是
A.由图可知:T1<T2,且该反应为吸热反应 B.T1时该反应的平衡常数K=7.2
C.前10min甲、乙、丙三个容器中A的反应速率:v(A)甲=v(A)乙<v(A)丙
D.平衡时A的质量m:m乙<m甲<m丙
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,正确的是( )
A.铝溶解在NaOH溶液中:2Al+2OH-+6H2O===2[Al(OH)4]-+3H2↑
B.氨水滴入AlCl3溶液中:Al3++3OH-===Al(OH)3↓
C.MgO溶于稀盐酸中:O2-+2H+===H2O
D.Al(OH)3溶于稀硫酸中:OH-+H+===H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com