
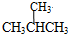 和
和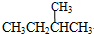 ;⑦
;⑦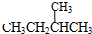 和
和
分析 (1)具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素;
(2)有机化合物中具有同一通式、组成上相差一个或多个某种原子团、在结构与性质上相似的化合物系列;
(3)具有相同分子式而结构不同的化合物互为同分异构体;
(4)同素异形体是同种元素形成的不同单质.
解答 解:⑤乙烯为烯烃,乙烷为烷烃,两者既不是同位素、也不是同系物、同分异构体、同素异形体,
(1)③16O、17O和18O质子数都为8,中子数分别为8、9、10,为氧元素的不同核素,互为同位素,
故答案为:③;
(2)④CH4和CH3CH2CH3,具有同一通式CnH2n+2、组成上相差一个一个-CH2-,属于同系物,⑥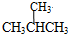 和
和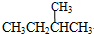 具有同一通式CnH2n+2、组成上相差一个一个-CH2-,属于同系物,
具有同一通式CnH2n+2、组成上相差一个一个-CH2-,属于同系物,
故答案为:④⑥;
(3)⑦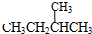 (异戊烷)和
(异戊烷)和 (新戊烷)分子式都为C5H12具有相同分子式而结构不同,互为同分异构体,
(新戊烷)分子式都为C5H12具有相同分子式而结构不同,互为同分异构体,
故答案为:⑦;
(4)①金刚石与石墨,是由碳元素组成不同单质,属于同素异形体,②氧气(O2)与臭氧(O3),由氧元素组成不同单质,属于同素异形体,
故答案为:①②;
点评 本题主要考查了同位素,同系物,同分异构体,同素异形体的定义,在判断时要抓住各自的研究对象分别为:原子、有机化合物、化合物、单质,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
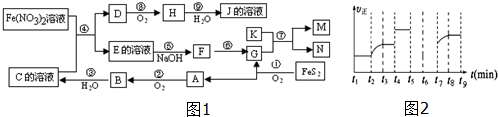
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
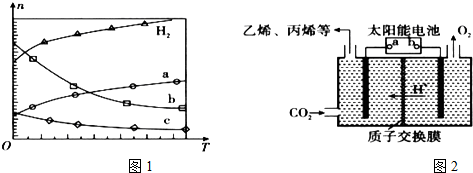
时间(min) 浓度(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,将1.12L Cl2溶于水,转移电子数为0.05NA | |
| B. | 将含等物质的量的KHCO3和Ba(OH)2溶液混合,离子方程式为:HCO3-+Ba2++OH-=BaCO3↓+H2O | |
| C. | 常温下,由水电离出的H+浓度为10-13mol•L-1的溶液中,Fe2+、Cl-、Na+、NO3-一定能大量共存 | |
| D. | 葡萄糖(C6H12O6)溶液中:SO42-、MnO4-、K+、H+可以大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
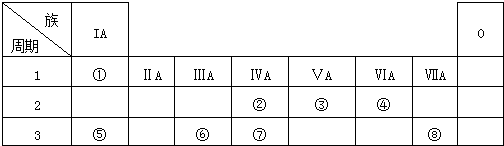
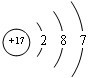 .
.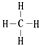 ,②和⑦的气态氢化物的稳定性相比,其中较弱的是SiH4 (用该氢化物的化学式表示).
,②和⑦的气态氢化物的稳定性相比,其中较弱的是SiH4 (用该氢化物的化学式表示).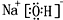 ,形成的晶体是离子晶体.
,形成的晶体是离子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④正确 | B. | ①③正确 | C. | ②④正确 | D. | 只有①正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com