
有关元素X、Y、Z、W的信息如下:
元素 | 有关信息 |
X | 原子半径为0.074 nm,其氢化物的结构模型可表示为: |
Y | 原子半径为0.102 nm,其原子核外电子排布为: |
Z | 人体中必需微量元素中含量最多,体内缺失会引起贫血 |
W | 所在主族序数与所在周期序数之差为4 |
请回答下列问题:
(1)W在元素周期表中的位置是 。
(2)Y与W相比,非金属性较强的是 (填元素符号),下列事实能证明这一结论的是 (填字母)。
a.W元素氢化物的稳定性大于Y元素氢化物的稳定性
b.W元素氢化物水溶液的酸性强于Y元素氢化物水溶液的酸性
c.W元素的单质能与Y元素的氢化物反应,置换出Y单质
d.W的最高价含氧酸比Y的最高价含氧酸的酸性强
(3)Z元素和X元素可形成离子Z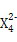 ,含该离子的盐是优良的绿色消毒剂和无机絮凝剂。
,含该离子的盐是优良的绿色消毒剂和无机絮凝剂。
①Z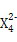 具有强氧化性,能杀菌消毒,还原产物是Z3+。
具有强氧化性,能杀菌消毒,还原产物是Z3+。
②含该离子的盐用作絮凝剂的原因是(用离子方程式和简要的文字说明) 。
(1)第3周期ⅦA族 (2)Cl a、c、d
(3)Fe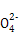 的还原产物为Fe3+,能发生水解反应,Fe3++3H2O
的还原产物为Fe3+,能发生水解反应,Fe3++3H2O Fe(OH)3(胶体)+ 3H+ ,生成的氢氧化铁胶体有吸附作用,起到净水作用
Fe(OH)3(胶体)+ 3H+ ,生成的氢氧化铁胶体有吸附作用,起到净水作用
【解析】由X的氢化物的结构模型可知X为O;由Y的原子核外电子排布可知a=2,b=6,即Y为S;根据表中Z的有关信息可知Z为Fe;又因W所在主族序数与所在周期序数之差为4,可推知W应为Cl,故(1)Cl在第3周期ⅦA族;(2)非金属强弱的判断方法有:气态氢化物的稳定性,其最高价含氧酸的酸性强弱、非金属之间的置换反应,故a、c、d正确;(3)Z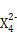 即Fe
即Fe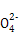 的还原产物为Fe3+,能发生水解反应,Fe3++3H2O
的还原产物为Fe3+,能发生水解反应,Fe3++3H2O Fe(OH)3(胶体)+3H+,生成的Fe(OH)3胶体具有吸附作用,起到净水作用。
Fe(OH)3(胶体)+3H+,生成的Fe(OH)3胶体具有吸附作用,起到净水作用。


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源:2014高考化学二轮专题突破 专题七化学反应与能量练习卷(解析版) 题型:选择题
某一化学反应在不同条件下的能量变化曲线如下图所示。下列说法正确的是( )
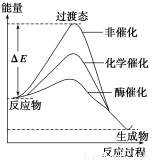
A.化学催化比酶催化的效果好
B.使用不同催化剂可以改变反应的热效应
C.使用不同催化剂可以改变反应的能耗
D.反应物的总能量低于生成物的总能量
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题8电化学原理练习卷(解析版) 题型:选择题
如图所示,将铁棒和石墨棒插入1 L 1 mol·L-1食盐水中。下列说法正确的是( )
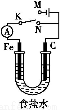
A.若电键K与N连接,铁被保护不会腐蚀
B.若电键K与N连接,正极反应式是:4OH--4e-=2H2O+O2↑
C.若电键K与M连接,将石墨棒换成铜棒,可实现铁棒上镀铜
D.若电键K与M连接,当两极共产生28 L(标准状况)气体时,生成了1 mol NaOH
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题6化学反应速率和化学平衡练习卷(解析版) 题型:填空题
T ℃、2 L密闭容器中某一反应在不同时刻的各物质的量如图所示(E为固体,其余为气体)。回答下列问题。
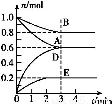
(1)写出该反应的化学方程式: 。
(2)反应开始至3 min时,用D表示的平均反应速率为 mol·L-1·min-1。
(3)T ℃时,该反应的化学平衡常数K= 。
(4)第6 min时,保持温度不变,将容器的体积缩小至原来的一半,重新达到平衡后,D的体积分数为 。
(5)另有一个2 L的密闭容器,T ℃、某一时刻,容器中各物质的物质的量如表所示。
物质 | A | B | D | E |
物质的量(mol) | 0.8 | 1.0 | 0.4 | 0.2 |
此时v(正) v(逆)(填“大于”、“等于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题6化学反应速率和化学平衡练习卷(解析版) 题型:选择题
煤气是生活中常用的燃料,制取水煤气的反应为C(s)+H2O(g) CO(g)+H2(g)。该反应在一容积可变的密闭容器中进行时,改变下列条件会对反应速率产生影响的是( )
CO(g)+H2(g)。该反应在一容积可变的密闭容器中进行时,改变下列条件会对反应速率产生影响的是( )
①增加碳的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大 ④保持压强不变,充入N2使体系体积增大
A.①② B.②③ C.②④ D.①④
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题5物质结构 元素周期律练习卷(解析版) 题型:选择题
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是( )
A.Y元素最高价氧化物对应的水化物化学式为H2YO4
B.原子半径由大到小的顺序为:Z>Y>W
C.X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定
D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1∶2
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题4化学反应中的能量变化练习卷(解析版) 题型:选择题
用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2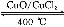 2Cl2+2H2O
2Cl2+2H2O
已知:Ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
Ⅱ.
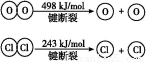
判断下列说法正确的是( )
A.反应A的ΔH>-115.6 kJ/mol
B.断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为32 kJ
C.H2O中H—O键比HCl中H—Cl键弱
D.由Ⅱ中的数据判断氯元素的非金属性比氧元素强
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题3氧化还原反应 离子反应练习卷(解析版) 题型:选择题
下列工业生产的反应原理不涉及氧化还原反应的是( )
A.钢铁厂高炉炼铁
B.工业上以氨气为原料用氨碱法生产纯碱
C.硝酸厂以氨气为原料制取硝酸
D.氯碱厂利用氯化钠生产氯气和烧碱
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题13物质结构与性质选修3练习卷(解析版) 题型:填空题
元素H、C、N、O、F都是重要的非金属元素,Fe、Cu是应用非常广泛的金属。
(1)Fe元素基态原子的核外电子排布式为 。
(2)C、H元素形成的化合物分子中共有16个电子,该分子中σ键与π键的个数比为 。
(3)C、N、O三种元素的第一电离能由大到小的顺序为(用元素符号表示) 。
(4)在测定HF的相对分子质量时,实验测得值一般高于理论值,其主要原因是 。
(5)C、N两元素形成的化合物C3N4形成的原子晶体,结构类似金刚石,甚至硬度超过金刚石,其原因是 。
(6)如图为石墨晶胞结构示意图,该晶胞中含有C原子的个数为 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com