
【题目】下列化合物只含有共价键的是( )
A.MgCl2B.KClC.NaClD.HCl
科目:高中化学 来源: 题型:
【题目】I.一定量的液态化合物XY2,在一定量的氧气中恰好完全燃烧,其化学方程式:XY2(l)+3O2(g)![]() XO2(g)+2YO2(g) (l代表液体,g代表气体)
XO2(g)+2YO2(g) (l代表液体,g代表气体)
冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56 g·L-1。
(1)观察反应前后气体的化学计量数,可得反应前氧气的体积是__________。
(2)化合物XY2的摩尔质量是__________。
(3)若XY2分子中X、Y两元素质量比是3:16,则X、Y两元素分别为__________和__________(填元素符号)。
II.常温下,将20.0 g质量分数为14.0 %的KNO3溶液跟30.0 g质量分数为24.0 %的KNO3溶液混合,得到密度为1.15 gcm﹣3的混合溶液。计算:
(1)混合后溶液的质量分数___________。
(2)混合后溶液的物质的量浓度____________(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
B. FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2=2Fe3++2H2O
C. 用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
D. 电解MgCl2水溶液的离子方程式:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是 ( )
A. 已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
B. 已知C(s)+O2(g)=CO2(g) ΔH1 C(s)+1/2O2(g)=CO(g) ΔH2;则ΔH2>ΔH1
C. 已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol
D. 放热过程(ΔH<0)或熵增加(ΔS> 0)的过程一定是自发的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用质量、形状均相同的锌片与下列条件下的稀硫酸反应时,化学反应速率最快的是( )
A.20℃1mol/L稀硫酸B.30℃1mol/L稀硫酸
C.20℃2mol/L稀硫酸D.30℃2mol/L稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2。
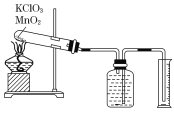
实验步骤如下:
①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95 g。
②连接好实验装置,检查装置的气密性。
③加热,开始反应,直到不再有气体产生为止。
④测量排入量筒中水的体积为285.0 mL,换算成标准状况下氧气的体积为279.7 mL.
⑤准确称量试管和残留物的质量为15.55 g。
根据上述实验过程,回答下列问题:
(1)如何检查装置的气密性?____________________________________________________________________________。
(2)试管中发生的化学反应方程式为:_______________________________________。
(3)以下是测量收集到气体体积必须包括的几个步骤:
①调整量筒的高度使广口瓶和量筒内的液面高度相同
②使试管和广口瓶内气体都冷却至室温
③读取量筒内液体的体积
这三步操作的正确顺序是___________(请填写步骤代码)。
进行③的实验操作时,若仰视读数,则读取氧气的体积________(填“偏大”、“偏小”或“无影响”)。
(4)实验过程中产生氧气的物质的量是________mol;实验测得氧气的摩尔体积是________(保留小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究氨气的还原性,某同学设计了下列实验装置( 其中夹持装置略去),在实验室中进行实验探究。回答下列问题:
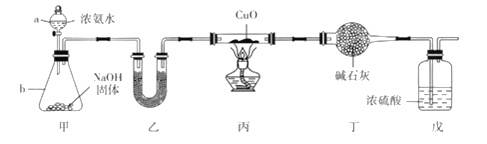
(1)仪器b的名称是_____________________,试解释该装置中产生NH3的原理:____________。
(2)装置乙中盛有的试剂名称是__________________。
(3)装置戊中浓硫酸的作用是_______________________________________________。
(4)+1价Cu 在酸性环境中不稳定,可发生反应:Cu2O+2H+==Cu2++Cu + H2O。某同学取上述反应后玻璃管内的物质于试管中,加入稀硫酸,振荡后发现溶液为蓝色,且试管底部有红色Cu,他得出结论:NH3还原CuO生成Cu2O。该同学的判断是否正确?________(填“正确”或“不正确”),理由是__________________________________________________________________。
(5)已知装置丙的玻璃管内CuO粉末为mg,实验结束后测得玻璃管内固体粉末为n g,若CuO 完全被还原 为 Cu,则 m:n=______;写出玻璃管内发生反应的化学方程式:__________________。装置丁中的干燥管增重为_______g(用含m 或n 的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com