
【题目】如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀.如表中液体X和固体Y的组合,不符合题意的是( )
① | ② | ③ | ④ | |
X | 水 | 水 | 稀硫酸 | 双氧水 |
Y | 硝酸铵 | 氢氧化钠 | 氯化钠 | 二氧化锰 |
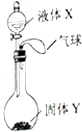
A.①③
B.②④
C.①②
D.③④
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案科目:高中化学 来源: 题型:
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
A | B | C | D | |
实验 | 用CCl4提取 溴水中的Br2 | 除去氢氧化铁 胶体中的氯化钠 | 从KI和I2的固体混合物中回收I2 | 配制100 mL0.1 mol·L-1 NaCl溶液 |
装置或 仪器 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2C(s)+O2(g)===2CO(g) ΔH=-Q1kJ·mol-1;
C(s)+O2(g)===CO2(g) ΔH=-Q2kJ·mol-1;
S(s)+O2(g)===SO2(g) ΔH=-Q3kJ·mol-1。
CO与镍反应会造成镍催化剂中毒,为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫,则该反应的热化学方程式为 ( )
A. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(2Q1-2Q2+Q3) kJ·mol-1
B. S(s)+2CO(g)===SO2(g)+2C(s) ΔH=(Q1-Q3) kJ·mol-1
C. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(Q1-2Q2+Q3) kJ·mol-1
D. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(2Q1-Q2+2Q3) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,H2(g) + CO2(g) ![]() H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
起始浓度 | 甲 | 乙 | 丙 |
C(H2)/ mol·l-1 | 0.010 | 0.020 | 0.020 |
C(CO2)/ mol·l-1 | 0.010 | 0.010 | 0.020 |
下列判断不正确的是
A. 平衡时,乙中CO2 的转化率大于60%
B. 平衡时,甲和丙中H2 的转化率均是60%
C. 平衡时,丙中C(CO2)是甲中的2倍,是0.012 mol·l-1
D. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组顺序的排列正确的是
A. 最高正价:P<S<Cl<Ar B. 热稳定性:H2O>HF>HCl
C. 酸性强弱:HNO3<H2CO3<H3PO4 D. 还原性 F- <Cl-<Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol·L-1醋酸溶液加水稀释,下列说法正确的是( )
A. 溶液中c(OH-)和c(H+)都减小 B. 溶液中c(H+)增大
C. 醋酸电离平衡向左移动 D. 溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是学习和研究化学物质及其变化的一种常用的科学方法。
(1)下列4组物质中均有一种物质的主要化学性质与其他3种不同。
A、CaO、Na2O、CO2、MgO B、CH3COOH、H2SO4、Ba(OH)2、HNO3
C、H2、Cl2、P、Cu D、HCl、CH3CH2OH、H2SO4、HNO3
①写出D组中不同于其他三种的物质的化学式:________。
②A组中的一种物质与B组中的—种物质反应的量不同产物有所不同。写出这两种物质反应有沉淀产生的离子反应方程式:_______。
③C组中Cu在一定条件下可与H2、Cl2、P等化合。写出 CuH在Cl2中燃烧的化学方程式:_________________。
(2)NaOH、Na2CO3、NaA1O2溶液都具有碱性。向500mL由NaOH、Na2CO3、NaA1O2组成的混合溶液中滴加0.2molL-1盐酸,所消耗盐酸体积如图所示,回答下列问题:
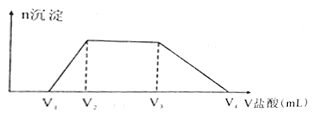
①写出加盐酸V1至 V2段反应的离子方程式:___________。
②用 36.5%(密度为1.19gmL-1) 的浓盐酸配制945mL0.2molL-1盐酸,需要量取的浓盐酸体积为_________________。
③若V1=50 mL,V2=100 mL,V3=200 mL,则V4= ______。原混合溶液中NaOH、Na2CO3、NaA1O2的物质的量之比为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com