
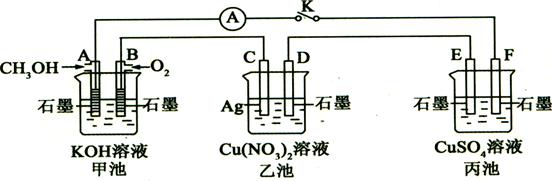
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(0H)2CO3 |


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源:不详 题型:填空题

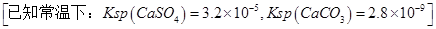 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
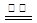 KIO3+3H2↑。下列有关说法不正确的是
KIO3+3H2↑。下列有关说法不正确的是| A.电解时,石墨作阳极,不锈钢作阴极 |
| B.电解时的阳极电极反应式:I-?6e-+3H2O = IO3-+6H+ |
| C.当电解过程中转移3 mol e-时,理论上可制得KIO3 107 g |
| D.电解一段时间后,电解质溶液的pH变小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.废弃的干电池不能随意丢弃,但可以土埋处理 |
| B.马口铁(镀锡铁)镀层破损后即失去保护作用 |
| C.不能将铁制自来水管与铜制水龙头连接使用 |
| D.电化学腐蚀过程中存在电极反应,产生微电流 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 (在反应前后La、Ni的化合价为0),其电池的反应通常表示为:
(在反应前后La、Ni的化合价为0),其电池的反应通常表示为: LaNi5+6Ni(OH)2
LaNi5+6Ni(OH)2| A.放电时电子流入储氢合金电极 |
B.放电时1mol 失去6mol电子 失去6mol电子 |
| C.放电时正极反应为NiOOH +H2O-e-= Ni(OH)2+OH- |
| D.充电时外接电源的正极应该接在储氢合金的电极上 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.① | B.①②④ | C.①②③ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
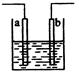
| A.a、b不可能是同种材料的电极 |
| B.该装置可能是电解池,电解质溶液为稀盐酸 |
| C.该装置可能是原电池,电解质溶液为稀盐酸 |
| D.该装置可看作是铜-锌原电池,电解质溶液是稀硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe-2e-==Fe2+ | B.2H++2e-==H2 ↑ |
| C.4OH--4e-==2H2O+O2↑ | D.2H2O+O2+4e-==4OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
D.图d中,工作时NH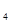 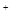 的移动方向为由里向外 的移动方向为由里向外 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com