
科目:高中化学 来源: 题型:
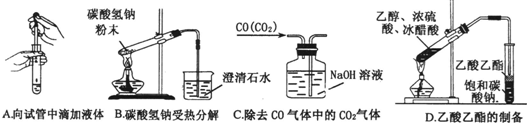
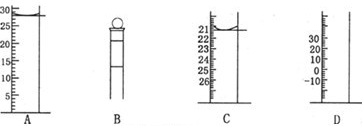
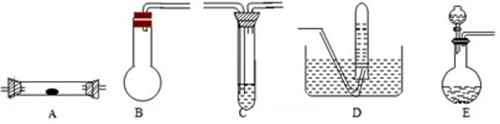
查看答案和解析>>
科目:高中化学 来源: 题型:
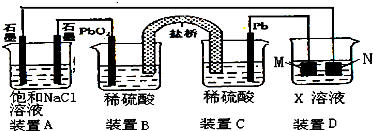
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| △ |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)某厂废水中含KCN,其浓度为650 mg·L-1。现用氯氧化法处理,发生如下反应(其中N的化合价为-3):KCN+2KOH+Cl2![]() KOCN+2KCl+H2O
KOCN+2KCl+H2O
被氧化的元素为___________。
(2)投入过量的液氯,可将氰酸盐进一步氧化为无毒的稳定物质。在横线上填写生成的无毒稳定物质,在方框内填写配平化学计量数:
□KOCN+□KOH+□Cl2——□KCl+□_________+□________+□H2O
(3)若处理上述废水20.0 L,使KCN完全转化为无毒物质,至少需液氯__________g。
查看答案和解析>>
科目:高中化学 来源:0103 期中题 题型:填空题
 +___H2O
+___H2O 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com