
 ;氯离子的电子式
;氯离子的电子式 .
.分析 (1)氯原子核外有17个电子,核外电子分为三个电子层;氯离子为阴离子,原子周围有8个电子;
(2)氯气与水反应生成HClO,HClO有漂白性;漂粉精的主要有效成分是次氯酸钙;
(3)硫酸与氯化钠反应生成HCl;
(4)氯气用氢氧化钠溶液吸收;根据元素的化合价变化判断;
(5)氯气是一种有着广泛用途的重要化工原料.
解答 解:(1)氯原子是17号元素,核外电子分为三个电子层,一层2个电子,二层8个电子.三层7个电子,原子结构示意图为 ;氯离子为阴离子,原子周围有8个电子,氯离子的电子式为:
;氯离子为阴离子,原子周围有8个电子,氯离子的电子式为: ;
;
故答案为: ;
; ;
;
(2)氯气与水反应生成HClO,HClO有漂白性,则氯气能使湿润的有色布条褪色,起到漂白作用的物质是次氯酸;漂粉精的主要有效成分是次氯酸钙,其化学式为Ca(ClO)2;
故答案为:次氯酸;Ca(ClO)2;
(3)实验室制备氯化氢气体利用原料氯化钠和浓硫酸加热反应生成氯化氢,微热时生成硫酸氢钠和氯化氢,反应的化学方程式为:NaCl+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HCl↑,
故答案为:NaCl+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HCl↑;
(4)氯气是有毒气体,能与氢氧化钠溶液反应,氯气用氢氧化钠溶液吸收;氯气与NaOH反应时,Cl元素的化合价既升高又降低,所以氯气既是氧化剂又是还原剂;
故答案为:NaOH溶液;c;
(5)氯气是一种有着广泛用途的重要化工原料,可用于制盐酸、漂白粉、有机溶剂与多种农药,
故答案为:制盐酸;漂白粉.
点评 本题考查了氯元素单质以及化合物的性质,题目难度不大,题目涉及的知识点较多,侧重于考查学生对基础知识的综合应用能力,注意把握氯气的性质和用途.


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学试卷(解析版) 题型:选择题
少量铁粉与100mL0.01mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10mL0.1mol/L盐酸.
A.①⑥⑦ B.③⑤⑧ C.③⑦⑧ D.⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 98g硫酸的摩尔数为1 mol | B. | 氧的摩尔质量为32g/mol | ||
| C. | 阿伏加德罗常数约为6.02×1023个 | D. | 某硫酸中H2SO4的质量分数为0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{V}{2}$L | B. | $\frac{V}{3}$L | C. | $\frac{5V}{6}$L | D. | VL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
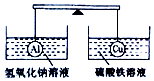 在杠杆的两端分别挂着质量和体积都相同的空心铝球和铜球,此时杠杆平衡.然后将两球分别浸没在氢氧化钠溶液和硫酸铁溶液中片刻,如图,则下列说法正确的是( )
在杠杆的两端分别挂着质量和体积都相同的空心铝球和铜球,此时杠杆平衡.然后将两球分别浸没在氢氧化钠溶液和硫酸铁溶液中片刻,如图,则下列说法正确的是( )| A. | 两烧杯中均无气泡产生 | B. | 左边烧杯中的溶液质量增加了 | ||
| C. | 在浸没过程中,杠杆始终保持平衡 | D. | 右边铜球质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
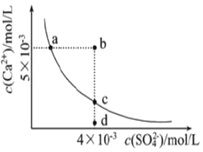
| A. | a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液 | |
| B. | a点对应的Ksp不等于c点对应的Ksp | |
| C. | b点将有沉淀生成,平衡后溶液中c(Ca2+)•c(SO42-)一定等于9×10-6 | |
| D. | 向d点溶液中加入适量CaCl2固体可以变成c点 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
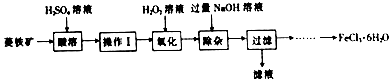
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com