
下列叙述正确的是 ( )
A.18 g水含有的电子数为9 NA
B.46g NO 和N2O4的混合物中所含氮原子个数为6.02×10
和N2O4的混合物中所含氮原子个数为6.02×10
C.0.1mol过氧化钠与足量的水反应,转移的电子数为 0.2NA
D.1L 0.3 mol/LNa2SO4溶液中,含有Na+和SO42- 总数为0.6 NA
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
除去Na2CO3 固体中混有少量NaHCO3的最佳方法是 ( )
A.加入适量盐酸 B.加入NaOH溶液
C.置于坩埚中加热 D.配成溶液后通入CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
(Ⅰ)根据反应4HCl(浓)+MnO2  MnCl2+Cl2↑+2H2O回答下列问题:
MnCl2+Cl2↑+2H2O回答下列问题:
(1)氧化剂是 , 氧化产物是 。
(2)HCl(浓)的作用是 。
(3)当有4mol HCl被氧化时,氧化产物的物质的量为 ,反应中转移的电子数为 。
(Ⅱ)丹砂的成分是HgS,汞单质和化合物在工业生产和科学研究上有其广泛用途。丹砂炼汞的反应包括以下两个反应:
反应Ⅰ:HgS+O2  Hg+SO2
Hg+SO2
反应Ⅱ:4HgS+4CaO  4Hg+3CaS+CaSO4
4Hg+3CaS+CaSO4
(1)反应Ⅰ中,还原产物是________,每生成1molSO2分子,转移电子数为________。
(2)反应Ⅱ中,HgS是________(填“氧化剂”、“还原剂”),用双线桥法标出反应Ⅱ中电子转移的方向和数目 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是( )
A. 金属与酸反应一定放出氢气 B. 含金属元素的离子一定是阳离子
C. 电离生成H+的化合物不一定是酸 D. 金属离子被还原一定得到金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象与氧化还原反应有关的是( )
A.铁和铝在浓硫酸和浓硝酸中发生钝化
B.向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成
C.NO2 通入水中,气体由红棕色逐渐转变为无色
D.硫酸铁溶液中滴加硫氰化钾溶液变红
查看答案和解析>>
科目:高中化学 来源: 题型:
常温常压下,把二氧化碳和一氧化氮的混合气体V mL缓缓通过足量的过氧化钠固体,气体体积缩小到 mL,则二氧化碳和一氧化氮的体积比不可能是( )(假设二氧化氮与过氧化钠不反应)A. 2:1 B. 3:2 C. 3:4 D. 5:4
mL,则二氧化碳和一氧化氮的体积比不可能是( )(假设二氧化氮与过氧化钠不反应)A. 2:1 B. 3:2 C. 3:4 D. 5:4
查看答案和解析>>
科目:高中化学 来源: 题型:
已知一定条件下A、B、C、D之间的转化关系如右图所示。下列说法正确的是( )
 A.若A为Fe,D为氢气,则B一定为酸
A.若A为Fe,D为氢气,则B一定为酸
B.若A、D为化合物,B为水,则C一定是气体单质
C.若A、B、C、D均为化合物,该反应一定属于复分解反应
D.若A、B、C、D均为10电子微粒,且C是可使湿润的红色石蕊试纸变蓝的气体,则D常温下一定呈液态
查看答案和解析>>
科目:高中化学 来源: 题型:
实验用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体,经历下列过程,Fe3+在pH=5时已完全沉淀,其中分析错误的是
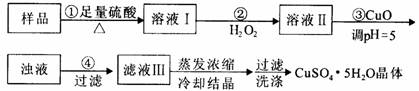
A.利用CuCO3替代CuO也可调节溶液的pH,不影响实验结果
B.步骤②中发生的主要反应为:H2O2+Fe2++2H+=Fe3++2H2O
C.洗涤晶体:向滤出晶体的漏斗中加少量水至浸没晶体,待自然流下后,重复2~3次
D.配制240 mL1mol/L的CuSO4溶液,需称量CuSO4·5H2O的质量为62.5g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com