
| A�����ʱ�������������ҺpH��С |
| B����ʹ�ù����д˵��Ҫ���ϲ���ˮ |
| C���ŵ�ʱNiO��OH���ڵ缫�Ϸ���������Ӧ |
| D�����ʱ������ӦΪNi��OH��2-e-+OH-�TNiO��OH��+H2O |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH��CH |
| B��CH2=CH2 |
| C��CH��C-CH3 |
| D��CH2=C��CH3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��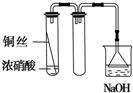 ʵ������ȡNO2 |
B�� ֤��CO2������ˮ |
C��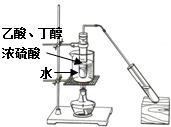 ʵ������ȡ���ᶡ�����е�126�棩 |
D��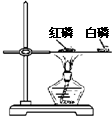 �ȽϺ���������Ż�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����Լ���SO32-ʱ����BaCl2��Һ��ϡHNO3�ữ |
| B��Ϊ��߸��������Һ�����������������Ὣ���������Һ�ữ |
| C��Ϊ�õ�MgCl2���壬��MgCl2��Һ�������ɼ��� |
| D���÷�̪��Һ�ɼ��𱥺�ʳ��ˮ�ͱ��ʹ�����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
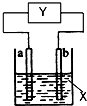 ��ͼװ����aΪ��ͭ����YΪ��·��δ֪���֣�XΪij��Һ�壬����˵����ȷ���ǣ�������
��ͼװ����aΪ��ͭ����YΪ��·��δ֪���֣�XΪij��Һ�壬����˵����ȷ���ǣ�������| b�� | X | Y���ֵ�· | a�ϵķ�Ӧ | |
| A | Zn | ϡH2SO4 | 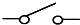 | 2H++2e��H2�� |
| B | ʯī | �ƾ� | 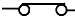 | Cu-2e��Cu2+ |
| C | ʯī | NaCl��Һ | 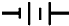 | 2H++2e��H2�� |
| D | ��ͭ | CuCl2��Һ | 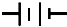 | Cu2++2e��Cu |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������� | ��ʼʱ�����ʵ����ʵ���/mol | �ﵽƽ��ʱ��ϵ�����ı仯/KJ | ||
| N2 | H2 | NH3 | ||
| �� | 1 | 3 | 0 | 46.3 |
| �� | 0 | 0 | 2 | Q1��0 |
| �� | 0.3 | 0.9 | 1.4 | Q2��0 |
| A��Q1=Q2=46.3KJ |
| B������NH3��ת���ʴ��ڢ���NH3��ת���� |
| C������ ����۷ֱ�ﵽƽ��ʱ��ƽ�ⳣ����ͬ����K��1 |
| D�������� �ٵķ�Ӧ������Ϊ���º�ѹ�н��У�Ͷ�������䣩���ﵽƽ��ʱ������ƽ��Ħ�������Ϻ��º���ʱ��С�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH4��C3H8 |
| B��CH4��C3H4 |
| C��C2H4��C3H4 |
| D��C2H4��C2H6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 mol�����μ�������ԭ��Ӧ��ת�Ƶĵ�����һ��Ϊ2NA |
| B����״���£�������Ȼ�ϵ�������һ����̼���干8.96L�������������г��ȼ��ʱ���������ķ�����Ϊ0.2NA |
| C����1 mol FeCl3����Һ��Fe3+�ĸ���ΪNA |
| D��1.8 g NH4+�к��еĵ�����Ϊ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ɵ�SO2����Ϊ0.3mol |
| B�����ɵ�SO2����Ϊ1.5mol |
| C�����ɵ�H2����Ϊ1.2mol |
| D�����ɵ�BaSO4����361.15g |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com